我们对人类病理生理学的机械性理解以及由此推动的药物研发和测试,面临着一个严峻的挑战:将有前景的体外实验结果转化为成功的临床结果。药物研发的高淘汰率,平均每种获批药物的研发成本至少为 28 亿美元,从一期临床试验到获得监管批准的成功率仅为约 6.7%,凸显了显著的转化差距。这一挑战在很大程度上归因于传统临床前模型的局限性。虽然传统的二维静态细胞培养在初始药物筛选中无处不在,但它们缺乏天然组织中复杂的结构、机械和生化线索,这一点在众多研究中已得到证实。生理相关的细胞外基质(extracellular matrix,ECM)相互作用、细胞异质性、动态生化梯度、机械应变、切应力和动态间质运输,是准确预测体内药物反应的关键决定因素。旨在弥补这一差距的动物模型,常常会引入物种特有的差异,比如药物代谢(例如细胞色素 P450 酶的变化)、转运蛋白表达(例如 P-糖蛋白)、免疫反应以及信号通路等方面的差异,从而限制了动物实验结果在人体生理学中的转化相关性。在评估分子跨生物屏障的转运时,这些局限性尤为明显。生物屏障——如血脑屏障(BBB)、肠上皮、肺泡毛细血管界面、胎盘屏障和肾小球滤过屏障——是动态的、具有选择性渗透性的界面,能够精确调节离子、小分子和生物大分子在组织间隔与全身循环之间的双向运输。这些屏障的生理相关模型对于推进我们对药代动力学过程(包括药物吸收、分布、代谢和排泄)的理解至关重要,同时也有助于阐明诸如神经退行性疾病、癌症转移和母胎疾病等广泛病理状况的机制基础。传统的体外模型往往无法复制这些动态界面中细胞和结构成分的复杂相互作用,从而导致对药物渗透性、疗效和潜在毒性的预测不准确。例如,缺乏相关细胞间相互作用(如星形胶质细胞 – 内皮细胞相互作用)和生理切应力的静态 BBB 模型可能会高估药物渗透,并且无法捕捉由转运蛋白介导的主动外排机制。此外,包括胎盘模型在内的几种体内动物模型由于物种特异性差异,无法模拟关键的人类生理和分子特征,从而限制了其转化相关性。与此同时,诸如欧盟的“3R”倡议之类的伦理和监管准则提倡在临床前研究中减少、优化和替代动物使用,这凸显了开发先进的与人类相关的体外平台的必要性。微生理系统(Microphysiological systems,MPS),包括器官芯片(organ-on-a-chip,OoC),已成为药物开发和生物医学研究领域的一项变革性技术,为传统的体外培养甚至体内动物模型提供了更准确且更具生理相关性的替代方案。这些模型通过整合三维组织结构、动态流体流动、可控微环境以及多种细胞类型的集成,重现了体内类似的微环境,能够模拟关键的生理过程,如营养物质运输、切应力、代谢活动以及免疫细胞相互作用。具体而言,微流体屏障模型通常由两个或多个通过半透膜分隔的通道组成,使研究人员能够研究生理界面的选择性渗透性、运输动力学和屏障完整性。先进的设计越来越多地融合了相关细胞类型的共培养(例如,血脑屏障模型中的星形胶质细胞、神经元和周细胞)、细胞外基质成分(例如,胶原蛋白、层粘连蛋白和纤连蛋白)以及微加工特征(例如,可灌注的微血管和微通道),以复制人体组织的结构和功能复杂性。近期已开始尝试将自动化和传感技术整合到体外屏障模型(OoC)平台中,包括用于跨上皮电阻、氧气和代谢物监测的电化学传感器,以及用于基于荧光的分子运输和溶解气体追踪的光学传感器。尽管这些方法代表着重要的进步,但大多数系统仍受限于部分自动化、单一参数传感、手动液体处理以及缺乏闭环反馈控制。此外,传感和采样通常仅限于屏障的一侧,这限制了在动态、非平衡条件下对运输进行的时间分辨分析。尽管微流控技术近来有所进步,但芯片上屏障模型的广泛应用和功能部署仍受制于技术复杂性、手动操作(包括缺乏自动流体处理和反馈控制)、时间分辨率有限以及动态梯度捕获不足等问题,这阻碍了其可重复性。一个关键且尚未解决的挑战在于准确模拟和量化非平衡分子传输现象,这涉及在异质流体组成和动态流动条件下同时发生的被动扩散、主动运输、对流和渗透力之间的复杂相互作用。重要的是,非平衡传输是肾脏、肺和血脑屏障等几个重要器官的基本特征,在这些器官中,精确调节的动态分子交换控制着诸如过滤、吸收和选择性渗透等关键生理功能。例如,肾脏的肾小球滤过屏障起着大小和电荷选择性被动过滤器的作用,允许小于约 15 – 30 kDa的分子进入尿液。尽管原生肾小球屏障的有效截留范围是动态且情境相关的,但这一大小范围为体外过滤模型提供了一个有用的生理参考。由于被截留的血浆蛋白产生的强大渗透力,准确预测过滤率仍然具有挑战性,这种渗透力会诱导溶剂拖拽,并能通过氢键和离子力等分子相互作用逆转溶质的运输。通常,芯片上的屏障模型是在专门设计的微流控装置内构建的,并且在屏障的两侧都缺乏传感和采样能力。由于没有这些传感能力,几乎不可能预测和量化非平衡分子在屏障两侧的传输情况,从而无法复制动态传输现象,也削弱了这些模型的预测能力和转化相关性。为应对这些挑战,我们提出了一种全自动微流控灌注平台,旨在提高分子运输研究中的生理保真度、操作稳健性和分析精度。该系统能够精确、自动地调节并进行时间分辨监测关键的物理化学参数,包括压力控制的流速、温度、溶解氧(DO)浓度和液体再循环,这些参数对于重现不同力在非平衡分子跨屏障界面运输中的同时相互作用至关重要。我们通过一项使用牛血清白蛋白(bovine serum albumin,BSA)和荧光素作为分子示踪剂的概念验证被动运输研究来验证平台性能,该研究展示了在模拟肾小球滤过生理相关条件下的半透膜两侧分子通量的受控、时间分辨定量。关键特性包括高精度压力驱动流量控制;带有容积传感器的双循环回路,具备故障保护功能;单向灌注;可编程的自动多试剂注射;在屏障两侧同步采样;以及用于连续监测溶解氧、流速、压力和温度的集成传感器。通过将自动化与多模态传感相结合,该平台能够实现对复杂物理化学环境的可重复、闭环控制,并推进了传感器驱动的微生理模型的发展,以研究非平衡传输和屏障功能障碍。
微流控硬件组件、制造及软件
该平台的机械设计是使用 SolidWorks 构建的。电子元件均从商业渠道采购(OB1 MK4 压力流量控制器,4 通道 0 – 2000 毫巴,12/1 MUX 微流体分配阀,MUX Wire阀控制器,3/2-way切换阀,MFS4 数字流量传感器,量程 30 – 1000 微升/分钟;法国 Elveflow 公司),除了液位传感器是内部设计的,通过集成 Zisenisc ZCT-YOF07 电容式传感器(法国 Farnell 公司)实现,以及光学氧(O2)传感器由德国 Scientific Bioprocessing 公司商业化生产。该平台的外壳使用 FDM 打印机(熔融沉积成型),Ultimaker S5(荷兰)打印而成,采用通用且坚韧的聚乳酸(PLA)。模块之间的流体通道由聚四氟乙烯(PTFE)管制成,外径分别为 1/16 英寸和 1/32 英寸,内径分别为 1/32 英寸和 300 微米。气动通道由聚氨酯管制成,外径 4 毫米,内径 2.5 毫米。管路和模块通过聚醚醚酮(PEEK)和全氟烷氧基(PFA)¼ 英寸 – 28 号外螺纹至 1/16 英寸外径和 1/32 英寸外径的管路连接器、乙烯 – 四氟乙烯(ETFE)¼ 英寸 – 28 号内螺纹至鲁尔外螺纹连接器、聚丙烯¼ 英寸 – 28 号旋转至 3/32 英寸内径的带卡箍连接器、迷你鲁尔至 1/32 英寸外径的管路插入式连接器以及硅胶套管进行连接。为完成该平台,使用了压力帽(法国 Elveflow 公司)、加热单元(中国 SADIJPR 公司)和循环桥单元(Microfluidics Innovation Center, France)。集成平台的控制软件和用户界面使用 LabVIEW(2022 年第三季度发布版)进行开发。
微流控芯片的制造与组装
微流控模块(流量控制、再循环、氧传感、注射、收集)的单独测试是通过使用两个活接头而非芯片,并借助 Elveflow 智能接口软件(ESI,Elveflow,法国)来控制系统完成的。而集成模块的完整平台的特性测试则是通过使用微流控芯片以及专用软件来控制和同步系统来完成的。
分子转运检测法
运输实验使用荧光素作为小分子示踪剂,使用牛血清白蛋白(BSA)作为代表性的大分子,因其在血液中含量丰富。平台概念验证实验使用的是 10 千道尔顿截留分子量的硝酸纤维素透析管,在潮湿条件下保存。将膜组装在树脂芯片中,各腔室用 1×PBS 缓冲液填充,如上所述。在连接芯片之前,整个流体系统用 PBS 充满,对于每个回路,70 毫升的 PBS 分别分配到两个储液器中(储液器 1 中 45 毫升,储液器 2 中 25 毫升)。进行运输实验时,将芯片放置成膜垂直方向。为注入回路 1(荧光素和 BSA;1 毫升)准备一份等分试样,以使注入后的起始浓度为 20 微克/毫升荧光素和 1 毫克/毫升 BSA。组装好的芯片连接到微流控平台上,并置于恒温箱中。将流速设置为回路 1 为 400 微升/分钟,回路 2 为 200 微升/分钟(400:200 比例)或每个回路均为 400 微升/分钟(400:400 比例)。启动了自动运输分析,在此期间从两个回路中分别采集了 1 个基线样本和 19 个运输样本(120 微升;每隔 10 分钟)。通过荧光光谱法(激发/发射:485/528 纳米)对每个采集样本中的荧光素浓度进行定量,同时使用 BioTek 公司的 Synergy 2 HTX 板式读数仪在 280 纳米处通过紫外吸光度监测 BSA 的运输情况。运输分析基于积分质量平衡原理(质量和流量守恒),假设载体流体(PBS)或示踪化合物(BSA 和荧光素)没有额外的来源或汇。在连续流动条件下,假设电路 1 的储液器中示踪剂浓度固定,建立了一组微分方程来平衡入口和出口流量以及相应的示踪剂质量通量。在稳态下,假设膜或电路内示踪剂没有净积累;因此,微流控芯片各腔室内示踪剂浓度的时间导数近似为零。
统计分析
采用学生双样本 t 检验(假设均值相等)确定统计学意义;相应地给出了 p 值。
结果
这项工作描述了从模块化组件开发微流控灌注平台并进行概念验证测试的过程,该平台用于实现运输测定的自动化,即能够测试化合物在类似于生物模拟屏障的半透膜上的运输情况。该平台旨在满足协议和技术标准化及自动化的需要,同时保持通用性和适应性,以适用于各种应用,即不受微流控芯片几何形状、膜特性以及特定细胞模型的限制。该平台的核心设计为两条流体通道(电路 1 和电路 2),由一个主流体单元独立控制(图 1A、B)。这两条电路连接到一个仿生屏障微流控芯片的两侧,该芯片置于一个集成的热控室中(图 1A、B)。这种配置满足了监测示踪化合物对仿生膜的影响和/或其跨膜运输的关键要求。该微流控平台集成了功能模块,可控制每个电路的独立液体循环、向电路 1 注入化合物并混合,以及从电路 1 和 2 进行时间分辨的样本采集(图 1C – E)。仪器模块采用颜色编码,以区分两条流体通道,并有助于组装和操作。每条电路中的溶解氧都持续进行在线监测。构建了一个热控室来控制分子运输区的温度(在环境温度和 50°C 之间),例如,如果需要,可为在微流控芯片的膜上同时培养细胞提供选择。
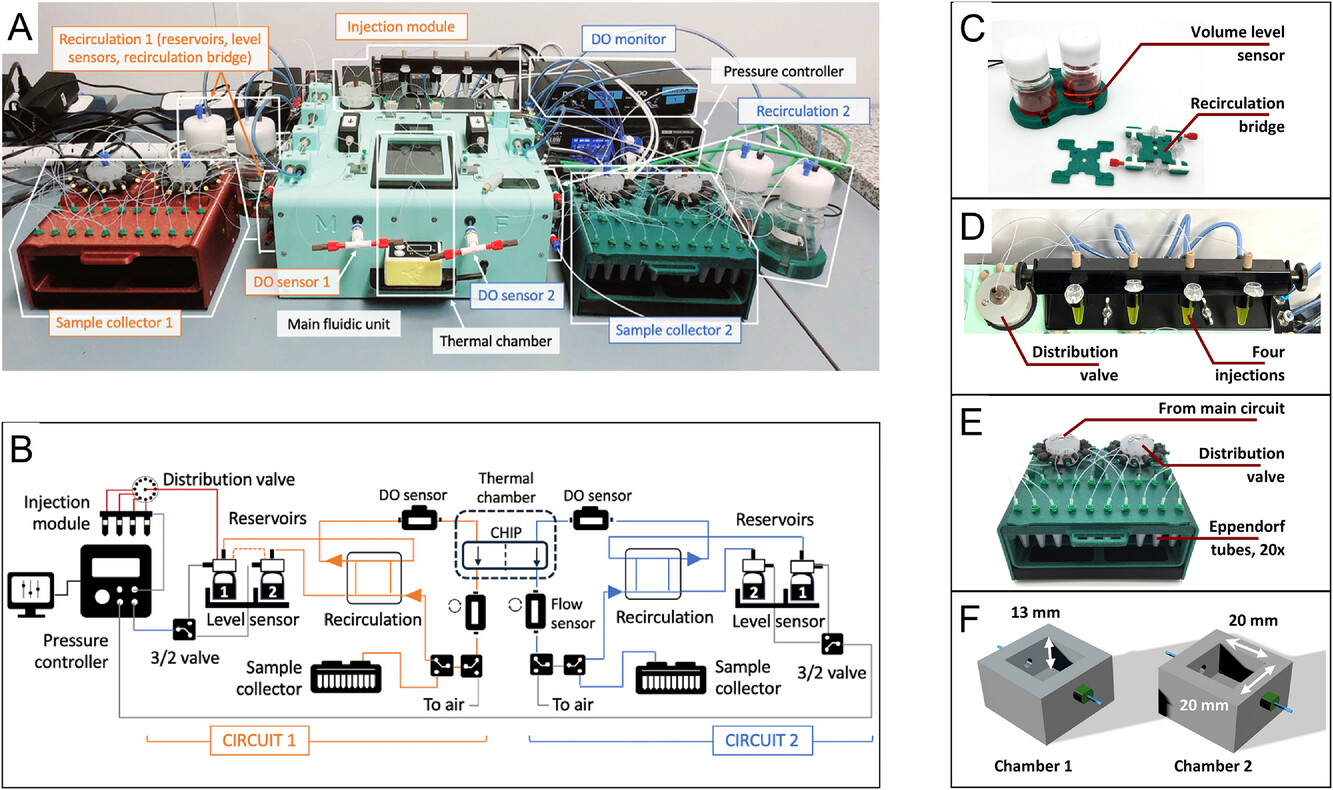
图1:用于自动化分子运输检测的微流控平台。(A)整个微流控平台的视图,由多个模块组成(深红色:电路 1,深绿色:电路 2,浅绿色:主流体电路模块)。(B)两个电路中的流体路径示意图(橙色、蓝色)。(C)传感器化循环模块由带集成体积液位传感器的烧瓶支架和单向循环桥组成。这些模块的工作原理在图 3 中详细说明。(D)注射模块由四个 Eppendorf 支架和一个 MUX 分配旋转阀组成。该模块的工作原理在图 4 中进一步详细说明。(E)适用于多达 20 个样本的样本收集模块。(F)芯片示意图。流体流动由压力驱动的流量控制器(OB1 MK4,Elveflow)和两个串联的热流量传感器控制,这两个传感器分别与独立的比例 – 积分 – 微分(PID)反馈回路相连,以实现自动流量控制。为了最大限度地提高平台的通用性,并且不受流速和灌注时间长度的影响,液体处理路径被整合为在每个回路的两个容器(此处为 100 毫升的肖特玻璃瓶)之间循环。任何时候,一个容器处于加压(流动)状态,而另一个处于未加压(收集)状态,在活动容器中的液体即将耗尽之前(即正在被推动液体的容器),两者会交替。每个回路的循环流动路径由一系列 3/2-way切换阀控制,这些阀能够自动独立地在两个容器之间切换(图 1B)。设计了体积“故障安全”液位传感器,当活动容器中剩余的液体量达到最小值时,向主控制单元发出信号。这会触发活动容器的自动切换,通过切换阀门的位置来开始对现在已满的容器进行加压(图 1B,C)。流体路由采用了一个由四个止回阀和四个 T 形接头组成的方形再循环桥,确保液体在微流控芯片中的流动始终是单向的。使用了一个分配阀,以便能够将多达四种不同的测试化合物按程序顺序注入电路 1 的储液器 1(图 1B、D)。测试化合物架与 Eppendorf 管兼容,因此,注入体积范围为 10 至 1500 微升。开发了两个自动样品收集单元,以便能够定时收集多达 40 个样品,它们位于微流控芯片之后的直线上。每个样品收集器都装有两个集成分配阀,并包含一个可拆卸的架子,可容纳多达 20 个 Eppendorf 管大小的试管,这些试管排列在带有流体管连接端口的可扣紧盖子下方。该平台设计为能与多种商用或自制的膜芯片兼容,这些芯片置于一个热控室中。这里所用的微流控芯片由两个相同的矩形腔室组成,腔室配有迷你鲁尔接头,用于与微流控管路进行流体连接(图 1F)。
软件设计与功能
在 LabVIEW 中开发了专用软件,以实现Sequence序列调度和流量流型的编程,从而实现整个实验的自动化(图 2A)。用户界面将实验参数(用户参数和保存的配置)和系统参数所需的用户输入分别划分到不同的选项卡和字段中。该软件同步了与所有控制流的仪器(压力控制器、旋转阀和 3/2-way切换阀控制器)之间的通信,以实现集成功能的自动化,即在两个回路(通过芯片的两个独立腔室)中进行介质的单向循环、将化合物注入回路 1 并混合以及从回路 1 和 2 定时采集样本。
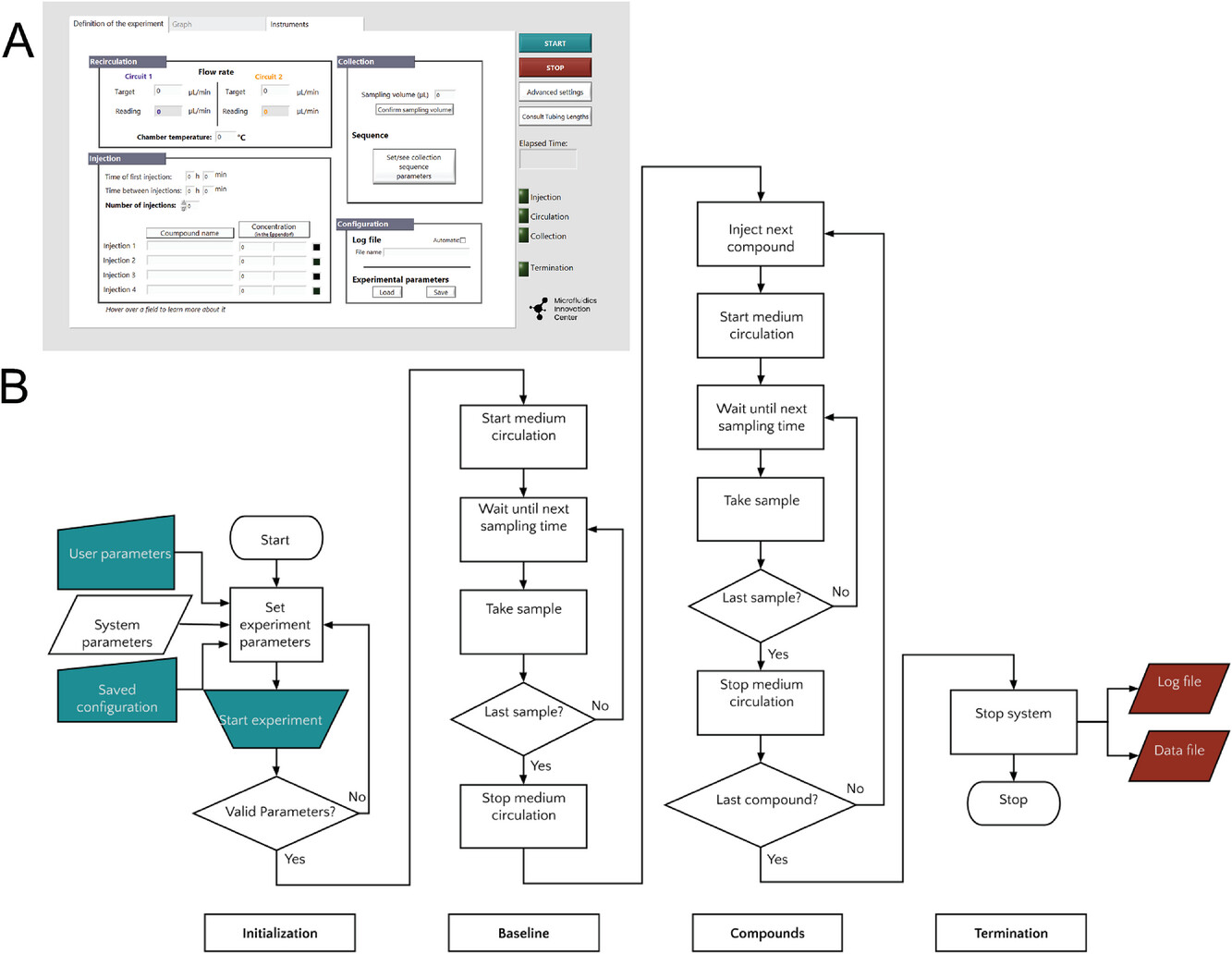
图2:平台操作软件。(A)“实验定义”选项卡中用户输入参数概览。(B)运输测定决策树。软件的用户输入(绿色形状)和输出(红色形状)已标明。流程图概述了四个实验阶段:初始化、基线获取、给定化合物/浓度的获取(根据要求重复多次)以及终止。该软件依照决策树(图 2B)控制仪器。设计了运行初始化步骤,用于识别并拒绝不合理的实验参数,并向操作员发出警报,例如步骤时间安排不合理以及未提供所用化合物的信息。实验启动后,程序会安排进入基线阶段。这被定义为根据两个流体回路的输入流参数对微流控芯片进行灌注,且不添加测试化合物,并收集用户定义数量的样本,例如从每个回路收集一个或多个样本作为基线参考。在基线样本收集完成后,系统被编程为停止流体流动,自动注入第一种化合物,并使回路 1 的两个流体储液器的内容物均匀化。然后重新启动循环,软件被编程为按照用户设定的时间间隔收集样本。在为给定注入化合物采集最后一个样本后,系统被编程为继续注入下一种化合物(如果有的话),或者关闭与仪器的所有通信,并生成数据文件和日志文件。
模块稳定性和精度的表征
为了在使用压力驱动流体控制时保持微流控芯片内的单向流动,在每个回路中芯片前都设计并串联了一个再循环桥。通过两对平行的止回阀的特定朝向来引导流体路径,基于液体通过止回阀的单向流动(图 3A)。桥的对角连接到两个液体储液器,其余的角则与微流控芯片相连(图 1B)。在其中一个 T 型接头提供两个可能的流动方向的情况下,流体通过反压最小的止回阀循环。这种配置使得桥内有两种不同的流动路径,这取决于是哪个储液器(R1 或 R2)被加压。具体来说,从桥流向芯片的液流与储液器的来源无关,即液流从桥的一个角流出,无论哪个储液器被加压(如图所示的朝向,即左上角;图 3A)。同样,从芯片返回的液流总是从桥的一个角重新进入(右下角;图 3A)。
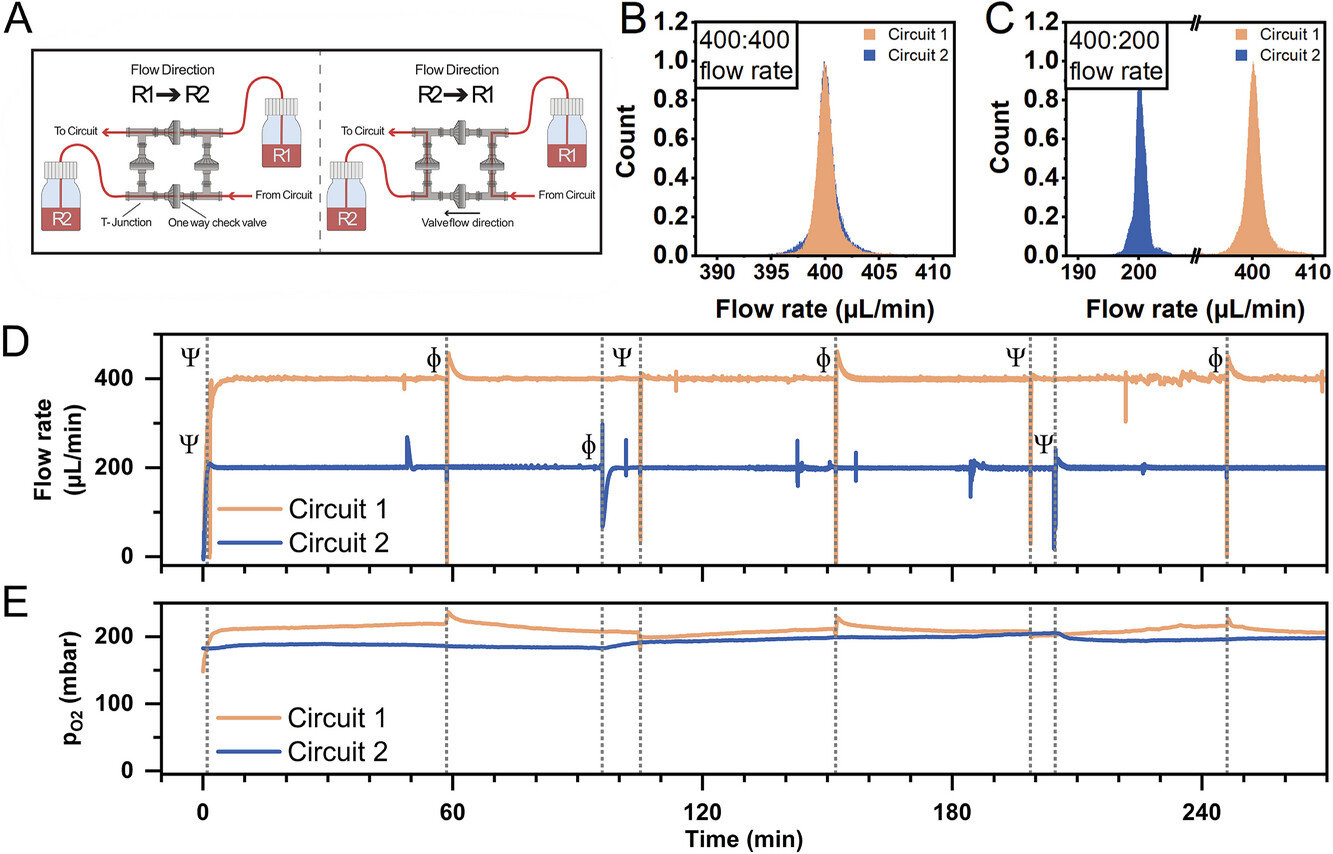
图3:流量控制和监测模块的性能。(A)在循环桥中存在两种可能的流路。液体从储液器 1(R1)或储液器 2(R2)流出,取决于哪个储液器正在加压。在两种情况下,液体均从桥的左上角单向流入回路,并从回路的右下角返回。(B)使用压力控制器软件在两个回路中设定流速为 400 µL/min 时的流速值的归一化直方图(回路 1,橙色;回路 2,蓝色)。(C)使用压力控制器软件在设定流速分别为 400 µL/min(回路 1,橙色)和 200 µL/min(回路 2,蓝色)时的流速值的归一化直方图。(D)使用压力控制器软件时的流速随时间变化曲线(回路 1,400 µL/min,橙色;回路 2,200 µL/min,蓝色)。交替对储液器 1(Ψ)或 2(ɸ)加压的情况已标明。(E)使用压力控制器软件时的 O2 分压随时间变化曲线(回路 1,400 µL/min,橙色;回路 2,200 µL/min,蓝色)。流体控制模块表现出稳定的流量调节能力、持续的再循环性能以及在不同系统条件下的运行适应性。压力驱动的流量控制器、流量传感器、液位传感器和再循环桥模块被整合起来,以控制两个独立回路的流量达 4.5 小时(图 3B – D)。对于两个回路,流量稳定并保持在目标值。针对不同流量比的实验,计算了记录流量(每秒采集一次)的归一化直方图:400:400 比例(两个回路均为 400 微升/分钟;图 3B)和 400:200 比例(回路 1 和回路 2 分别为 400 和 200 微升/分钟;图 3C)。在 400:200 比例下,稳定流量分别测量为 400.0 ± 0.5、200.0 ± 0.4 微升/分钟(回路 1 和回路 2),在 400:400 比例下,稳定流量分别测量为 400.0 ± 1.1、400.0 ± 1.3 微升/分钟(回路 1 和回路 2)。如上所述,设计了集成式储液器容积液位传感器,以实现每次仅对一个储液器进行交替加压,当检测到最低液位时自动触发气动系统切换,其功能得到了验证(图 3D)。正如预期的那样,在两个流路的流量曲线中观察到储液器加压切换时流量瞬间降至接近零。每次切换时都出现一个小峰值,表明反馈回路在起作用,以将流量稳定在目标值,这与 PID 控制系统一致。连续切换之间的间隔是恒定的(在 200 微升/分钟时为 105 分钟,在 400 微升/分钟时为 50 分钟),这说明了液位传感器的工作功能(图 3D)。对于两个流路,第一个储液器加压的持续时间与后续周期略有不同,这与操作员最初在两个储液器之间分配液体的情况相符。在同一个 4.5 小时的实验中,对两个回路中氧分压(pO2)的变化进行了测量(图 3E),并与流量(图 3D)同步,实验过程中 pO2 保持稳定(在 180 至 220 毫巴之间)。在两个回路中,pO2 均缓慢且小幅变化,与 1 号和 2 号储液器的交替切换同步,分别用符号 Ψ 和 Φ 表示(图 3D)。在自动化微流控运输检测中,一个关键的参数化步骤是将化合物加入一个回路中。这里所描述的平台被设计成能够自动进行多达四次独立的化合物注入。具体来说,注入序列被设定为将化合物加入回路 1 的两个储液器中的一个,然后将两个储液器的内容物离线混合,最后将液体在线导入整个回路和微流控芯片(图 1B 和 4A)。在每次注入之前,储液器 1(R1)的内容物会立即被排空到储液器 2(R2)中,之后化合物被注入 R1(图 4A 步骤 1)。然后,液体在 R1 和 R2 之间以高流速(> 100 毫升/分钟)来回循环,使内容物均匀(图 4A 步骤 2)。
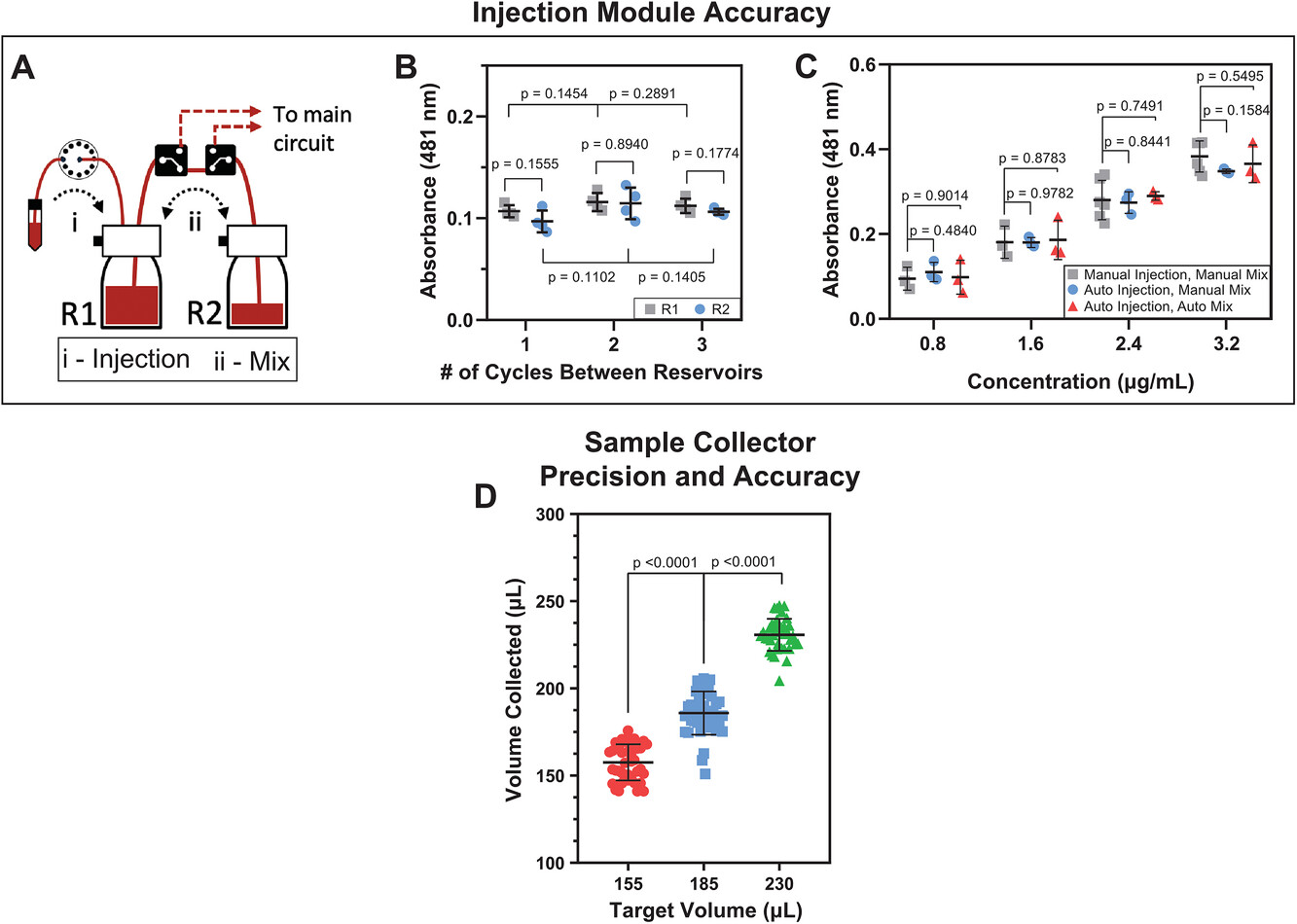
图4:注射和收集模块的性能。(A)注射模块工作原理:i)化合物被注入到回路 1 的储液器 1 中。ii)介质和化合物在回路 1 的储液器 1 和 2 之间来回循环,直至混合均匀。(B)储液器 1(黑色方块)和储液器 2(蓝色圆圈)中注入化合物的混合效率与来回循环次数的关系。(C)平台对连续注射的通用性:在手动注射和摇动(黑色方块)、使用微流控平台自动注射和手动摇动(蓝色圆圈)或自动注射和三个自动来回混合循环(红色三角形)的情况下,连续四次注射荧光素时储液器 1 中的吸光度(平均值 ± 标准差,n = 3 – 5)。(D)在三种独立的目标样本体积(155、185、220 微升)下,样本收集过程中的体积一致性(每种情况 n = 40)。p 值通过未配对 t 检验计算得出。为评估在连续往复混合循环后化合物均质化的有效性,使用水中的荧光素作为注入化合物进行了一系列测试。在电路 1 的 R1 和 R2 中,荧光素在一次往复循环后迅速与缓冲液均质化,这从两个储液器中相当的吸光度值得到了证明(图 4B)。对四次相同顺序的荧光素注入,测试了自动注入和混合与手动注入和摇晃相比的效率,并报告了储液器 1 的结果(图 4C)。自动和手动注入及混合方法的吸光度值相当,并且随着连续注入而线性增加,这表明自动注入和混合功能有效。该平台集成了两个样本采集模块,以实现按照操作员设定的时间间隔和样本量从两个回路中自动采集样本。通过在三个不同目标体积的完全自动化实验中进行采集,对性能和通用性进行了测试。采集管在采集前后进行称重,样本质量经密度校正(20°C 时 PBS 的密度为 1.005584 克/毫升)后以体积表示。所采集样本的平均体积均在目标值的 1.5% 以内(157 ± 10 微升,目标 155 微升;185 ± 12 微升,目标 185 微升;231 ± 9 微升,目标 230 微升;平均值 ± 标准差,每种情况 n = 40;图 4D)。
概念验证:用于分析半透膜屏障两侧物质传输动力学的自动化微流控系统
为证明该系统监测示踪剂在半透膜屏障两侧运输的能力,进行了概念验证实验。该实验旨在模拟诸如肾小球滤过屏障之类的屏障上的被动运输,使用了标称分子量截留值(molecular weight cut-off,MWCO)为 10 千道尔顿的半透性硝酸纤维素透析膜作为概念验证屏障。硝酸纤维素膜具有明确的孔隙率、低厚度和可重复的运输特性,适合在压力驱动灌注下研究尺寸选择性过滤和渗透运输。所选的 MWCO 保守地近似了肾小球的尺寸选择性,同时能够系统地研究被动运输和溶剂拖曳效应。重要的是,该平台架构不受膜类型限制,未来可适应不同器官系统相关的其他 MWCO 和屏障配置。该实验还测试了在集成流速和流体再循环控制下复合注射与样品采集的同步性(图 5)。评估了两种流速组合:400:400 和 400:200 微升/分钟(回路 1:回路 2)。所注射的化合物是牛血清白蛋白(66 千道尔顿)和荧光素(0.33 千道尔顿)的混合物。荧光素预计会穿过膜扩散(回路 1 到回路 2;图 5A),而牛血清白蛋白则不应穿过,从而在相反方向(回路 2 到回路 1)形成渗透梯度。
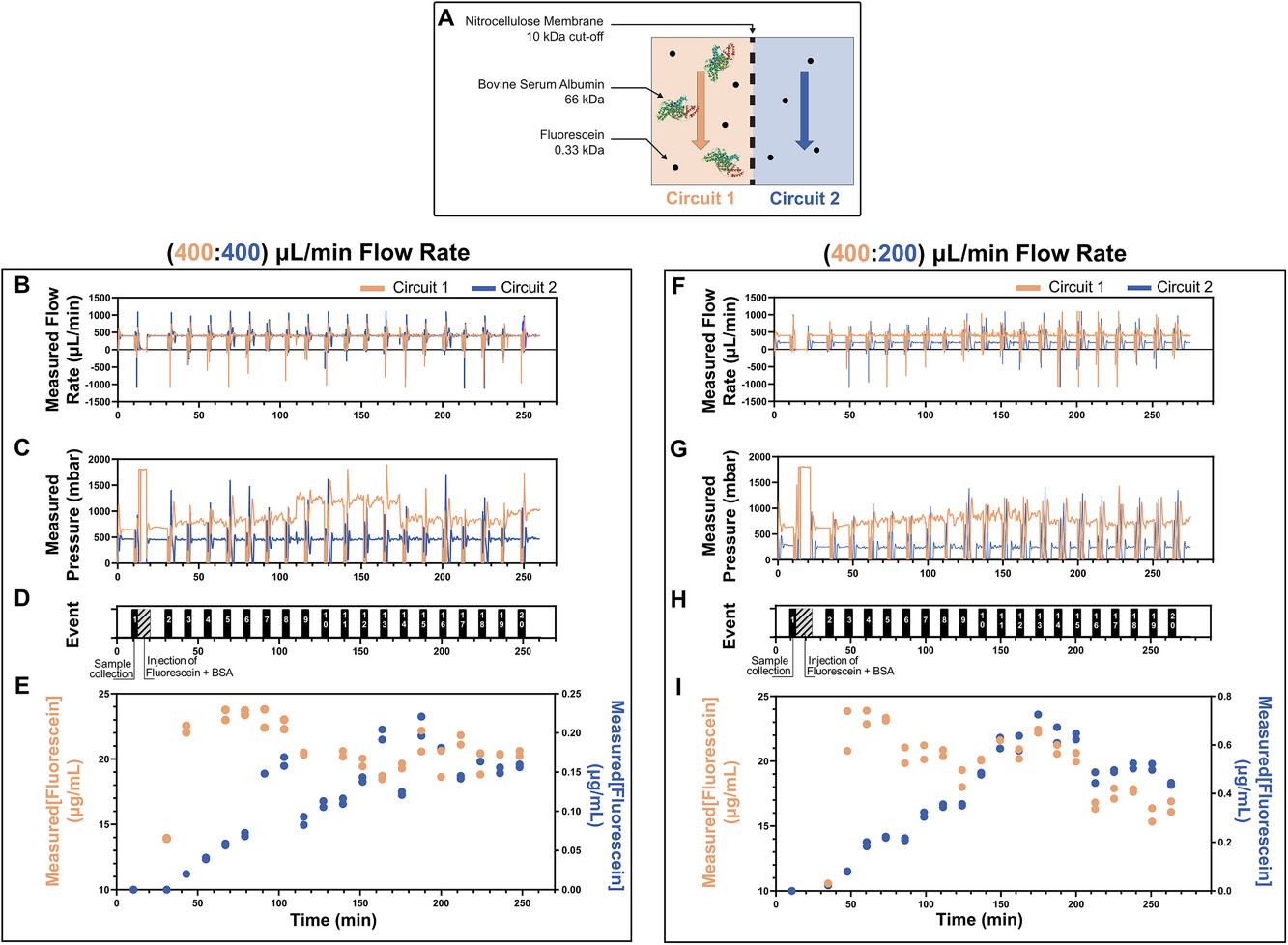
图5:在不同流速下对非平衡系统中分子传输的自动化微流控平台分析。(A)芯片内流体方向示意图。(B-I)展示整个平台性能,并证明其自动化在(400:400)微升/分钟(B-E)和(400:200)微升/分钟(F-I)流速比下,分子通过半透膜屏障传输动力学的概念验证。同步测量的流速、压力、注射和样品收集时间,以及在不同流速下电路 1 和电路 2 中测量的荧光素浓度。记录的流量(图 5B、F)、工作储液器压力(图 5C、G)以及事件序列(注入、收集;图 5D、H)在长达 4.5 小时的实验过程中进行了同步,该实验包括向 1 号回路注入一次化合物以及从每个回路收集 20 次样本。在循环 10 分钟后,从两个回路各采集一个样本作为基线。紧接着(t = 11 分钟),将目标化合物注入并混合到 1 号回路(最终储液器浓度为 20 微克/毫升荧光素和 1 毫克/毫升牛血清白蛋白),然后系统在加载介质的情况下开始循环。随后的 38 个样本(每个回路 19 个)每隔 10 分钟采集一次。在采集事件期间,每个回路的流量分别进行监测,以冲洗采集管路、抽取样本体积并清洗管路,其特征是压力和流量的快速变化。每次采集事件结束后,PID 算法会驱动压力快速稳定在目标流量,直至下一次采集事件。值得注意的是,在取样瞬间,流体即刻受到干扰,导致振荡压力变化衰减(图 3D 和图 5B、C、F、G)。由于取样间隔时间远大于这些扰动事件,因此这不会对膜沿面的剪切速率产生显著影响,这一点在计算流体动力学(CFD)建模中已观察到(数据未显示),也不会对累积化合物的转移动力学产生显著影响。分别采用紫外 – 可见光谱法和荧光光谱法测定了 20 个收集样本中 BSA 和荧光素的浓度(图 5E、I)。对于两种流速比,电路 1 中的荧光素水平逐渐降低,而电路 2 中的浓度则逐渐升高,这表明存在定向跨膜运输。然而,测量值表明,电路 1 中荧光素浓度的降低速度比电路 2 中浓度的升高速度快。这些结果与非平衡被动运输的原理相符,这种运输是由半透膜屏障两侧的渗透化合物的简单扩散浓度梯度之外的多种力驱动的(图 6A)。这种行为符合热力学原理:流体之间的化学势差不仅驱动渗透示踪剂穿过膜,还驱动反向渗透和压力差驱动的溶剂流动(携带),压力和流速的波动会加剧这种效应。因此,要计算跨膜的准确运输速率,必须考虑两个方向的运输质量。采用积分质量平衡原理[35, 38]精确表征了荧光素的传输动力学(图 6B、C)。传输动力学分析表明,在 400:200 微升/分钟的流速比下,电路 2 中荧光素的积累量显著高于 400:400 微升/分钟的流速比。这种差异与在较低流速下电路 2 中的停留时间增加相一致;然而,在当前条件下,无法区分这种增强的积累是由于流量限制传输还是仅仅由于停留时间延长所致。这些结果表明,传输效率对流量不对称性和停留时间敏感,但需要进一步的研究来区分这些因素的影响。值得注意的是,在电路 2 中未检测到 BSA,这表明,正如预期的那样,BSA 没有穿过膜(图 S2)。
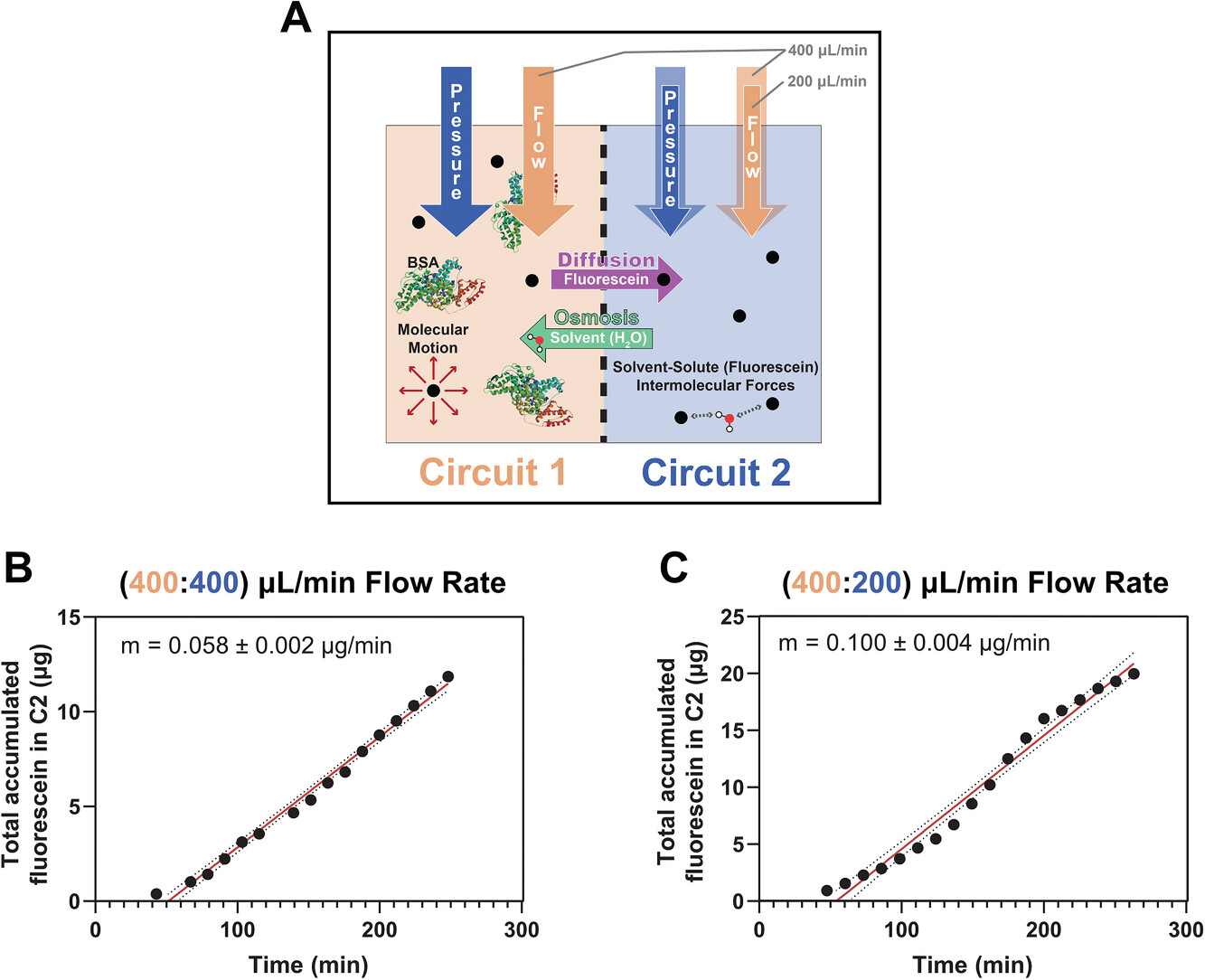
图6:根据图 5 中的流量和荧光素浓度数据计算出从回路 1 到回路 2 的荧光素传输速率。(A)描绘了影响荧光素从回路 1 被动传输到回路 2 的不同力的示意图。(B 和 C)在不同评估流速下,从回路 1 到回路 2 的总荧光素传输随时间的变化情况。观察到的小溶质的选择性通过表明,该微流控平台支持受控的、大小依赖的和流量敏感的分子传输,证实了其在组织模拟系统中模拟屏障功能和溶质交换方面的实用性。
讨论
我们开发了一种全自动化的微流控平台,该平台集成了高精度压力驱动流量控制、双循环回路及容积故障安全监测、可编程多试剂注射(10 – 1500 微升)、同步多腔室样本收集、实时溶解氧监测以及温度控制室。这一集成系统解决了当前器官芯片和微流控屏障模型的关键局限性,包括技术复杂性、操作者引入的变异性以及受限的时间分辨运输分析。选择压力驱动流是因为其具有高稳定性、响应性和可编程性,能够生成稳态和脉动流型,以模拟生理微环境。自动驱动和可编程序列调度的实施减少了人工干预,提高了可重复性,并支持实验室间的标准化。热室与商用和定制芯片(标准显微镜载玻片尺寸)兼容,主控模块设计可置于标准生物安全柜内,为未来活细胞应用中的无菌操作提供了可能。流量分布呈现出非正态特征,这归因于系统初始化和稳定阶段的包含。在这些过渡期间,超调和欠调事件导致了分布的偏态。孤立的瞬态偏差归因于热流量传感器对机械冲击或气泡的敏感性。尽管存在这些干扰,但在稳态运行期间,系统仍保持稳定的流量曲线。溶解氧传感器成功集成,实现了对其的实时监测。由于溶解氧与氧分压(PO2)以及工作流体中的绝对压力(Pabs)之间存在关系 DO(%)= 100×PO2/Pabs,因此在连续运行期间观察到的缓慢的 PO2 波动被归因于随着储液器排空 Pabs 的缓慢变化。该系统的一个关键特性是采用了电容式液位传感器,以确保每个储液器中的液体量保持在设定的阈值之上,防止空气进入和流量中断。这些传感器能够根据实际测量而非理论计算的液体量实时调整储液器的切换时间。这可以补偿由于传感器漂移、气泡、泄漏或逐渐生物污染而产生的微小流量偏差。测量的切换间隔与流速成适当比例,证实了体积跟踪逻辑的准确性。例如,流速减半时,切换事件之间的间隔大约增加了一倍,这与预期的线性关系相符。它们还为集成注射系统做出了贡献,该系统在化合物的注射和混合方面与手动操作一样高效,同时还具有提高重现性和防止泡沫形成(无需气泡或剧烈搅拌)的优点。这对于处理粘性液体和富含蛋白质的溶液(如添加了胎牛血清(FBS)的细胞培养基)来说是一项宝贵的资产。模块化采样架构支持对分子在屏障隔室内部及之间的分布和滞留情况进行时间分辨分析。这种设计有助于量化运输、化合物滞留以及由于膜吸附或管路相互作用导致的潜在损失。此类高分辨率的动力学数据对于体外评估药代动力学和屏障功能至关重要。实验结果和质量平衡分析与众所周知的生理学原理一致,即分子通过半透膜的运输并非仅由浓度梯度决定,而是由多种力的复杂相互作用所控制(图 6A)。这突显了在膜两侧同步进行双点浓度测量以解析对流和渗透贡献的关键重要性。该平台对于模拟非平衡生物系统(如人类肾脏)具有高度相关性,在这些系统中,动态和异质性流动条件普遍存在——这与流体体积和溶质质量固定的静态模型不同。由渗透力和溶质 – 溶剂相互作用引起的溶剂拖拽,可能会显著影响器官芯片和微生理系统模型中的运输行为。忽略这一现象可能会导致对体外数据生理相关性的误解。因此,在非平衡条件下准确量化运输动力学需要严格控制流动,并从仿生屏障的两侧同步采样。重要的是,尽管当前平台使用的是无细胞膜,但其架构完全兼容未来活细胞的整合,这将有助于研究主动运输、细胞屏障功能以及机械敏感反应。在采样过程中预计流体扰动会很小;然而,在未来的生物验证研究中,应考虑其对剪切敏感细胞层的潜在影响。
结论:
本研究介绍了一种全自动微流控平台,用于对屏障膜模型中分子跨膜转运进行时间分辨和生理相关的分析。该系统克服了现有微流控和器官芯片技术的关键局限性,包括手动流体处理、低重现性和有限的时间分辨率。通过整合压力驱动的流体控制、基于液位的双循环回路体积传感、可编程多试剂注射、同步多腔室采样、实时溶解氧监测以及热稳定化,该平台能够实现严格控制的长期灌注实验,且用户干预极少。自动化操作提高了实验的一致性,有助于在不同实验室间实现标准化。准确表征分子转运,同时考虑所有相关力(如溶剂拖曳力)的影响,对于将微流控数据转化为生理学背景至关重要。通过使用一种半透性仿生膜模型进行概念验证,该模型模拟了诸如肾小球滤过等生物运输过程,证明了该系统适用于动态分子运输分析。凭借在屏障两侧的先进且强大的采样能力,该平台可靠地捕获了动态运输动力学,并能够定量区分被动分子运输。该平台的未来版本旨在包含实时在线传感器,例如基于适配体的电化学传感器,以进一步提高定量分子运输的分辨率。这项技术在微生理系统领域取得了重大进展,弥合了实验室台式微流体与生理相关的体外模型之间的差距。其强大的自动化功能、实时监测能力和模块化架构使其成为在受控和可重复条件下进行临床前药物筛选、毒理学和屏障功能机制研究的强大工具。
参考文献:
Olivier Fournier, Miguel A. D. Neves, Théo Gavoille, Alan Morin, Beatriz Pais, etal. Advanced Sensor Research, 23 December 2025, 2751-1219.
