悬浮细胞,包括各种免疫细胞,如 T 细胞和 B 细胞,在生物学研究的众多领域中发挥着关键作用。与贴壁细胞不同,贴壁细胞需要附着在表面,而悬浮细胞则在培养基中自由漂浮,这与血液和淋巴等体液中的条件相似。这一特性在癌症研究中尤为重要,因为非贴壁免疫细胞是免疫治疗研究的核心。
免疫疗法利用患者自身的免疫系统来识别并消灭癌细胞。在免疫疗法的各种方法中,过继细胞疗法(ACT)因其个性化的特点而成为一种极具前景的策略,这有助于提高治疗效果。ACT 包括从患者体内分离免疫细胞,对其进行基因工程改造以表达特定的受体蛋白,在体外扩增这些细胞,然后将其重新注入患者体内,从而选择性地靶向癌细胞。
尽管具有潜力,但活化细胞疗法(ACT)在体外扩增 T 细胞时面临显著的技术挑战。传统的基于培养瓶的方法需要多次处理步骤,增加了污染的风险。尽管有效,但基于灌注的系统通常需要大量的培养基,有时超过 25 升,这使其资源消耗大。此外,较新的生物反应器技术虽然创新,但可能会无意中改变细胞动力学,从而影响细胞行为和治疗效果。
微流控技术为许多此类局限性提供了一个极具吸引力的解决方案。这种技术通常被称为“实验室的微型化”,它利用具有微米级腔室和通道的装置来创建受控环境。这些系统能够以受控的流速持续灌注新鲜的细胞培养基,为细胞提供营养物质并移除代谢废物。这些特性有助于建立长期培养体系、控制微环境以及对流出培养基进行实时分析。
芯片实验室(LOC)器件是微流控技术的核心,它将多种实验室功能集成到仅几平方厘米的紧凑平台上。这些设备由聚二甲基硅氧烷(PDMS)等生物相容性材料制成,可作为微反应器支持原核和真核细胞的生长,实现不同细胞类型的共培养。其小巧的尺寸减少了所需样本和试剂的体积,而其微通道的可定制设计能够适应特定的实验目标,包括多重检测。此外,LOC 器件还能够实现实验的并行化和结果的可重复性。
尽管微流控技术已在贴壁细胞中得到广泛应用,但悬浮细胞的操作却带来了独特的挑战。最显著的是,在长期灌注培养过程中进行培养基交换时存在细胞丢失的风险,这限制了专门用于体外 T 细胞扩增的自动化平台的发展。为解决这一问题,许多现有系统侧重于短期分析,依赖诸如物理夹持等策略,这可能会造成机械应力,或者具有不同的目标,比如形成球体。虽然存在更复杂的平台,但它们往往针对不相关的应用,例如微生物系统生物学的大规模扩展,或者涉及复杂的制造工艺,从而限制了其可及性。
建立长期的基于图像的文化体系会带来另一个瓶颈:管理和分析由此产生的大量数据。这一挑战因无标记图像处理的困难而加剧,无标记图像对于保持细胞活力至关重要。尽管传统的机器学习工具(例如在 Fiji 中广泛使用的可训练 WEKA 分割(TWS)插件或在 Matlab 中的自定义工作流)被广泛使用,但它们在动态培养环境中的准确性可能会受到伪影的影响。深度学习,如 U-Net 和高效的 YOLOv8 架构,已成为一种强大的替代方案。然而,其在 T 细胞成像中的应用主要集中在静态培养中的细胞分类或分析来自流式细胞术等非显微镜数据源的数据。这揭示了一个缺口,因为这些模型与用于量化长期 LOC 培养中 T 细胞增殖的既定基准的系统性评估尚未得到充分探索。
在这项研究中,我们通过展示一种集成的微流控系统来解决这些不足,该系统用于非贴壁细胞的长期培养,将自动灌注控制和图像采集与 LOC 器件相结合。图像分析采用基于深度学习的分割方法,并与 Fiji 的 TWS 插件进行了基准测试。对于采用这项技术的研究人员来说,一个核心问题是选择标准化的商用系统还是可适应的自制设备;然而,针对 T 细胞扩增的直接比较以指导这一决策尚缺乏。为解决这一问题,评估了两种替代方案:商用的 µ-Slide Spheroid Perfusion 设备(ibidi®,ibidi LOC”)和定制的 PDMS 设备(“PDMS LOC”),以评估它们各自在支持 T 细胞扩增方面的优势和局限性。
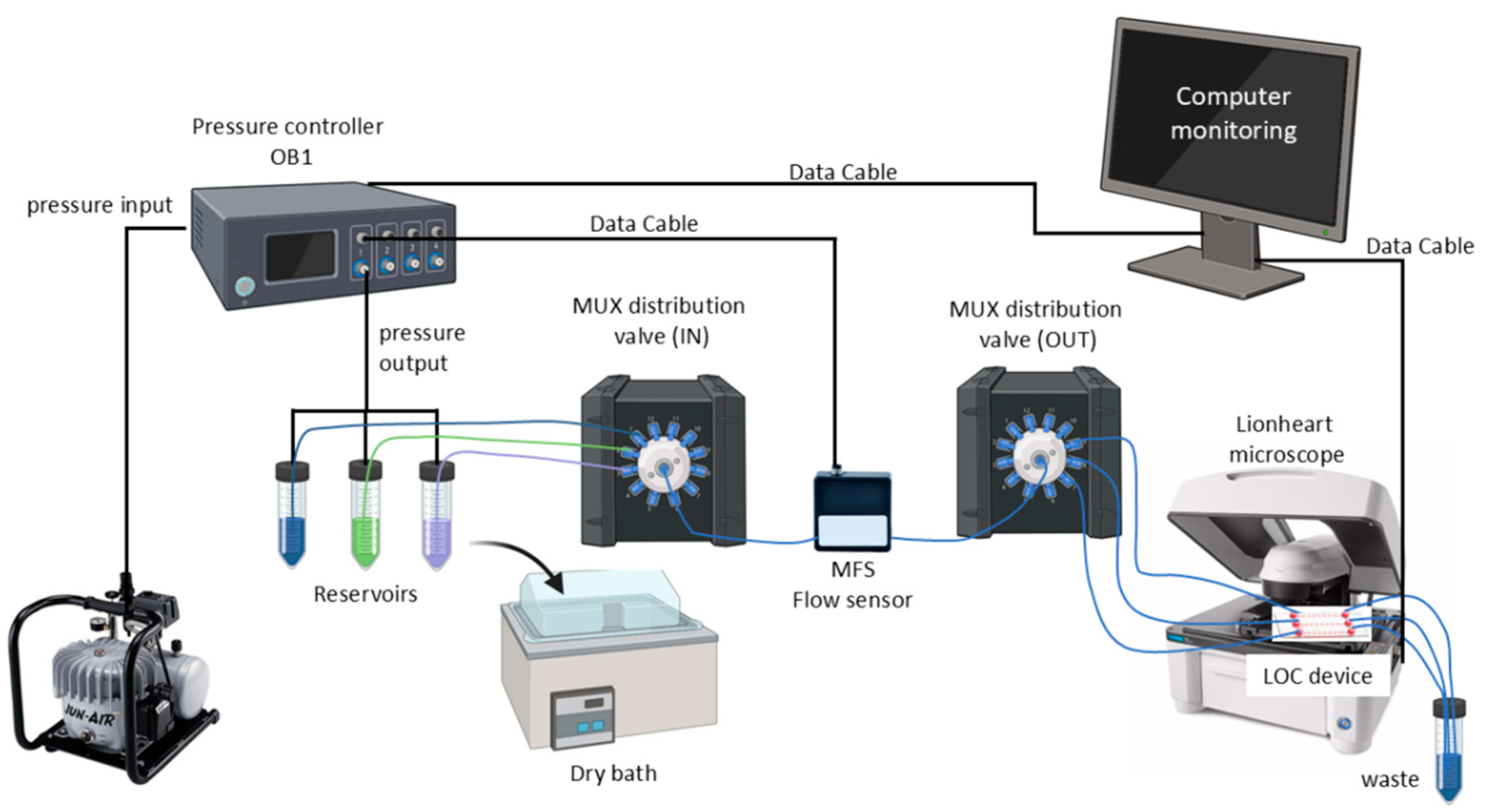
图 1. 微流控系统的示意图。该系统使用一个压力控制器(OB1,法国 Elvesys 公司),其接收来自空气压缩机的压力,并从正面连接到储液器(分别装有不同液体的 15 mL和 50 mL的 Falcon® 管)。从 MFS 流量传感器接收反馈,该传感器检测由施加压力产生的流速。液体通过连接到分配阀(称为 MUX)的管路进行传输。使用了两个阀,一个用于从储液器分配不同液体,另一个用于将液体分配到 LOC 器件。LOC 器件通过自动显微镜进行成像。所有设备均通过计算机进行监控。
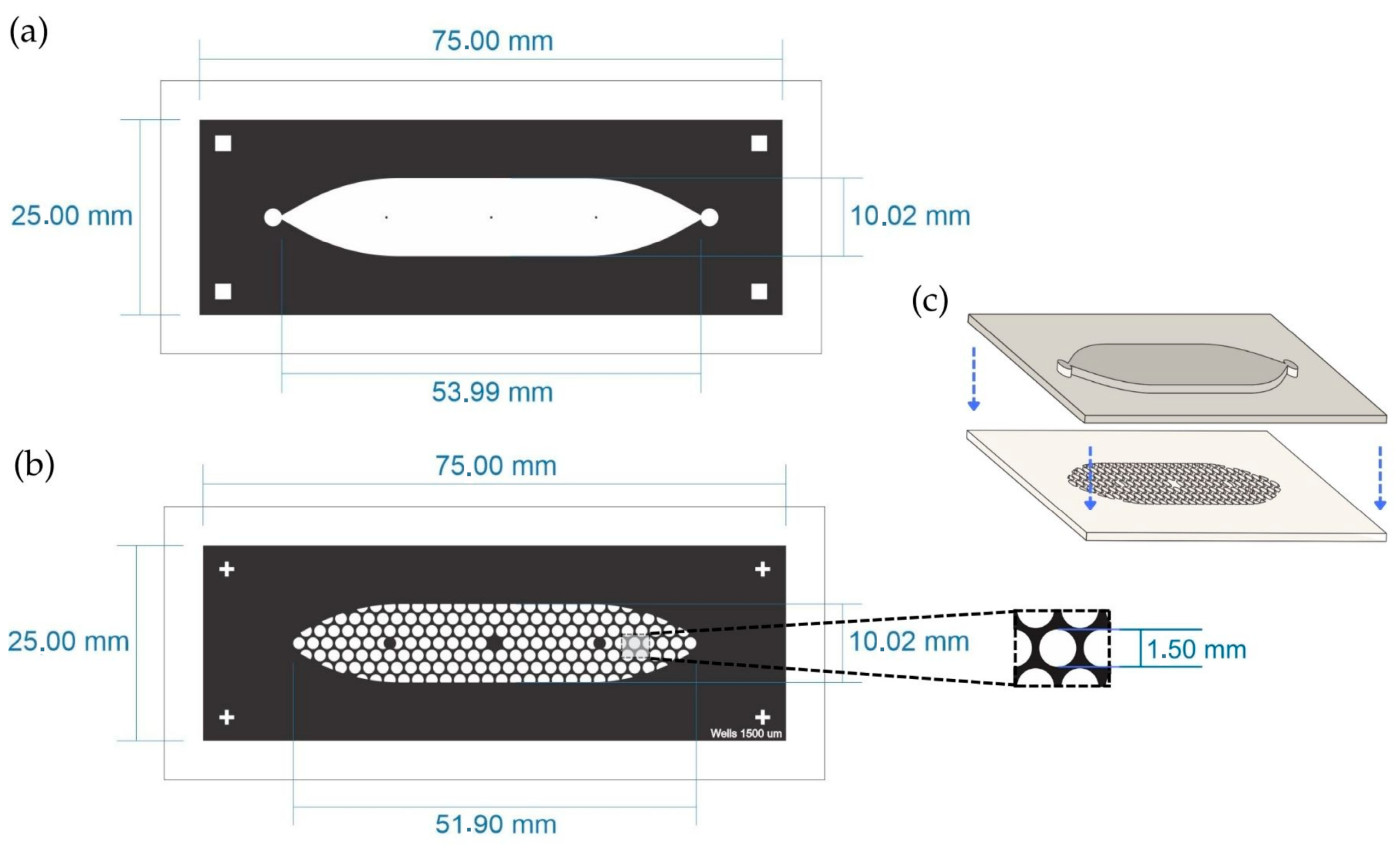
图 2. 聚二甲基硅氧烷(PDMS)芯片实验室(LOC)的示意图。(a)顶层包含长形蓄水池(53.99 毫米×10.02 毫米),带有入口和出口端口。(b)底层展示在蓄水池区域内呈六边形分布的圆形井阵列。插图显示了井的直径(1.5 毫米)。(c)通过等离子体键合将两层 PDMS 组装在一起。蓝色箭头指示两层组装的方向。
细胞系培养
使用由 Lighthouse Core Facility 提供的永生化人类 T 淋巴细胞系 Jurkat 对每个 LOC 装置的适用性进行了测试。Jurkat 细胞在 T-25 培养瓶中培养,培养基为完全高级 RPMI 1640 培养基,添加 4%胎牛血清(FBS)、1%青霉素 – 链霉素(10,000 单位/毫升青霉素,10,000 微克/毫升链霉素)和 1% L-谷氨酰胺(Gibco)。细胞在 37°C、5%二氧化碳的加湿环境中培养,每三天传代一次。
LOC 器件中的细胞接种与培养
在接种前,通过高压灭菌对 PDMS LOC 进行灭菌处理。将装置和预先补充的高级 RPMI 1640 培养基(Gibco)在 37°C 下孵育过夜。次日,先将培养基注入装置,随后注入细胞悬液。两者均需用移液管小心直接注入通道,确保完全覆盖区域,同时避免气泡形成。然后将装置在 37°C 下孵育 1 小时。
对于 ibidi LOC,测试了两种接种方案。在第一种方案中,先将盖玻片贴上,然后用微量移液管将无细胞的高级 RPMI 1640 培养基直接注入每个通道。在 37°C 下孵育 2 小时后,再次注入培养基以去除井和连接处的气泡。最后,将细胞悬液注入通道,孵育 1 小时后,用无细胞培养基填充鲁尔连接器。
在第二种方案中,用微量移液管将 2 微升细胞悬液分配到每个井中,确保底部无气泡残留。随后放置盖玻片,在 37°C 下孵育 1 小时后,注入无细胞培养基以填充每个通道并消除任何残留气泡。此时还填充了鲁尔接头。
另外,还进行了一项实验以评估表面涂层对细胞行为的影响。ibidi LOC 的通道用两种不同的涂层进行处理。一个通道涂有聚-L-赖氨酸(0.1 mg/mL),另一个涂有聚-D-赖氨酸(0.1 mg/mL),第三个通道未涂覆作为对照。完成涂层处理后,按照基于通道的方案接种 Jurkat 细胞,并使用选定的流动方案培养 150 小时。
使用自动细胞计数器(TC10 自动细胞计数器)和台盼蓝染料(0.40%,1.5 mL)测定细胞浓度。对于细胞接种,使用 5×105 个细胞/毫升的浓度以确保最佳生长条件。完成接种方案后,将微流控系统连接到 LOC 器件。在所有实验中,均使用了高级 RPMI 1640 培养基[添加了 4%胎牛血清(FBS)、1%青链霉素(每毫升含 10000 单位青霉素和 10000 微克链霉素)和 1% L-谷氨酰胺(Gibco)]。
流动条件下的细胞培养
为评估不同流动模式对细胞生长的影响,实验使用了 ibidi LOC,该装置可同时测试三种不同的条件。细胞按照基于通道的方案进行接种,随后施加了以下流动方案:静态对照——细胞在无流动和无培养基交换的条件下培养;恒定流动——以每分钟 2 μL的速率施加连续层流,该速率被选为系统能够稳定且精确测量的最低流速;间歇流动——由每分钟 10 μL的 5 分钟灌注和 2 小时 55 分钟的无流间隔组成,每 3 小时重复一次。
在其余实验中,对两个 LOC 装置均施加了每分钟 10 μL的流速。对于 PDMS LOC,每 2 小时施加 20 分钟的流速(总体积 200 μL)。对于 ibidi LOC,每 3 小时在每个通道施加 5 分钟的流速(总体积 50 μL)。采用不同的方案是因为 PDMS LOC 的通道体积较大,容易更快干燥。
成像
图像使用 Lionheart FX 自动显微镜获取。在 Gen5 软件 3.03 版本中配置了实验器件定义,由于每个 LOC 器件的尺寸不同,因此对每个器件都进行了单独调整。为了在长期实验中保持标准培养条件(37°C、5% CO2 和 90% 湿度),将台式培养箱(ibidi GmbH)连接到显微镜上。
对于 ibidi LOC,每 3 小时以 4 倍放大率拍摄明场图像,对于 PDMS LOC,则每 2 小时拍摄一次。成像时间表与分配方案同步。使用我们团队基于 U-Net 和 YOLOv8 架构开发的定制深度学习图像分析软件对图像进行分析。此外,还使用了 Fiji 的 TWS 插件来验证和比较结果。
使用 Fiji(Image J 1.54f)的 TWS 插件进行图像处理
从 ibidi LOC 捕获的图像被上传到 Fiji(Image J 1.54f)。为每个孔生成包含所有时间点的图像堆栈。使用编辑工具擦除孔外的背景。
使用适用于 Fiji 的 TWS 插件,该插件应用机器学习算法将图像分类为不同的类别,将细胞覆盖的区域与背景区分开来。使用一组八张图像对分类器进行训练,其中细胞覆盖的感兴趣区域(ROI)标记为一类,背景标记为另一类。
训练完成后,使用相同的分类器对每个图像堆栈进行分析,生成概率图。生成的图像由三个图层组成:孔外区域、背景和细胞覆盖区域。将这些图层分离,以隔离包含 ROI 的图层,然后自动阈值处理并转换为二值掩码。使用分析工具通过“分析颗粒”选项测量细胞覆盖的面积。结果以逗号分隔值(CSV)文件的形式保存。
基于深度学习的图像处理方法
深度学习是机器学习的一个分支,它利用多层人工神经网络来处理和学习数据。这些网络通过从有标签的数据集中学习来识别模式,其中每个数据点都与特定的标签或结果相关联。一旦训练完成,网络(通常称为模型)就能在新的、未标记的数据中识别相同的模式。在图像分析中,根据训练数据集中的标签和所使用的模型类型,可以执行各种任务,例如:
目标检测:识别图像中的物体并确定其位置,为每个检测到的物体提供边界框。
语义分割:将图像中的每个像素分类到预定义的类别中,将属于同一类别的所有像素归为一个实体。
实例分割:与语义分割类似,但增加了区分单个物体的能力。
对于 ibidi LOC 图像,使用了由先前生成并手动校正的注释组成的数据库,这些注释最初用于 TWS 分类器。采用了 U-Net 网络,其具有独特的 U 形结构,在二值语义分割任务中,尤其是在生物医学成像领域,已取得显著成功。使用 FastAI 框架进行训练,该框架已包含 U-Net 的实现。模型性能通过 Jaccard 指数(通常称为交并比或 IoU)进行评估。该指数衡量预测区域与标注区域的重叠程度,1 表示完全匹配,0 表示预测掩码与真实掩码之间没有重叠。
对于 PDMS LOC 图像,评估了 Ultralytics YOLOv8 实例分割模型。YOLOv8 架构是一种实时检测和分割模型,它优先考虑轻量级计算时间和高效资源利用,而非精度。尽管在这种环境中不需要实时推理,但高效的计算使其能够在没有图形处理单元(GPU)加速的情况下使用。这使得更多潜在用户能够使用更高级的分析方法,但代价是分割精度略有降低。
按照迭代自训练方案生成了 PDMS LOC 图像的数据集。最初,在由七张手动标注图像组成的小数据集上训练了一个起始模型。然后,使用该初始模型为未标注的数据集生成预测标签。经过人工验证和修正后,将预测结果添加到数据集中,从而能够训练出改进后的模型。这个循环反复迭代,直到生成一个稳健的数据集。为了评估 YOLOv8 架构的性能,计算了 IoU 值。
深度学习方法分析
U-Net 架构在包含 629 张来自 ibidi LOC 图像的数据集上进行了训练,其中 125 张图像用作验证集。对于这个二值分割任务,选择交并比(IoU)作为主要指标。训练完成后,所得模型在验证集上实现了平均 IoU 得分为 0.779,这反映了预测标签与真实标签之间的相似度。
对于 YOLOv8 架构,使用迭代自训练过程生成了一个包含 231 张来自 PDMS LOC 图像的数据集,其中 31 张图像用于验证。在该数据集上训练的最终 YOLOv8 模型在分割任务中对验证集实现了 0.873 的 IoU 得分。
在分析 PDMS LOC 图像时切换模型反映了对可能更适合不同环境和专业知识水平的替代深度学习模型的探索。在用于 YOLOv8 的相同数据集上还训练了一个额外的 U-Net 模型,其 IoU 得分为 0.912。尽管得分更高,但两个模型生成的掩码在对相同图像的分析中没有显著差异。为作对比,对使用 PDMS LOC 进行的一项实验中的四个孔进行了分析,该实验每个孔采集了 33 张图像(总计 132 张图像)。计算了两种模型中每个孔被掩码覆盖的面积百分比。尽管在某些情况下观察到掩码之间存在细微的视觉差异,如图 3 所示,但两种模型在孔面积覆盖上的平均差异仅为 0.69%,标准偏差为 0.60%。
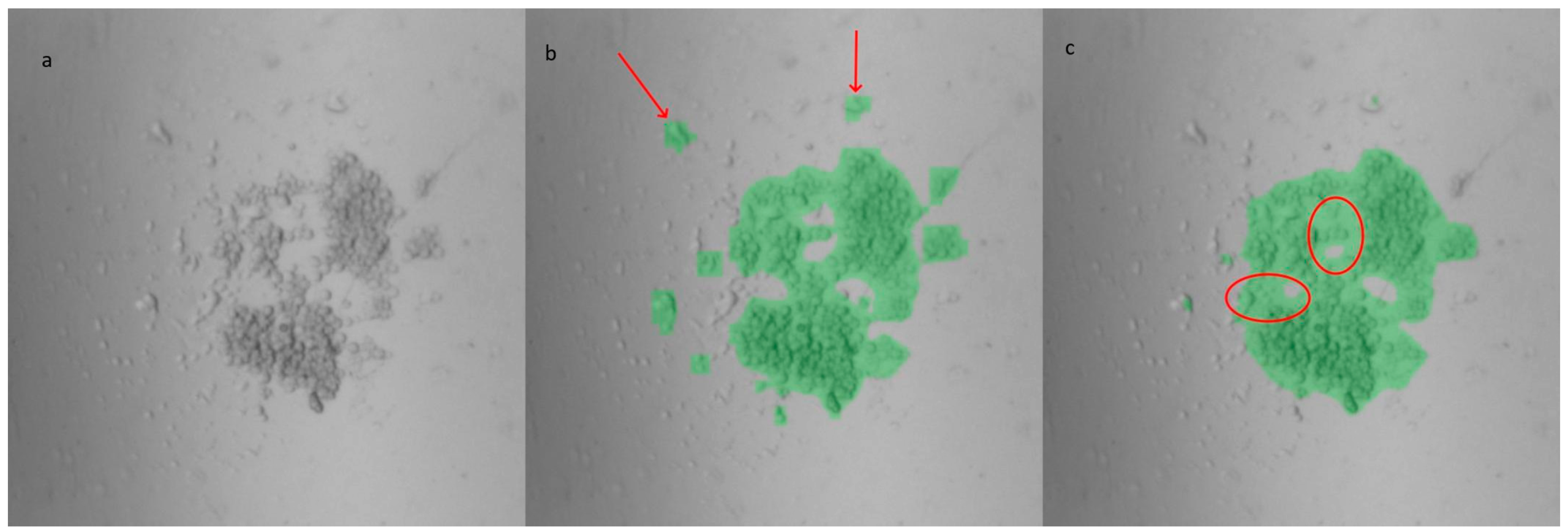
图 3. 由定制 PDMS LOC 图像生成的掩码:(a)原始图像,(b)YOLOv8m-segm 模型输出,(c)U-Net 模型输出。与 YOLOv8 相比,U-Net 掩码边缘更平滑,但包含更多背景(圆圈标注)。然而,U-Net 模型往往会遗漏位于中心较远的某些细胞,而这些细胞被 YOLOv8 掩码成功识别(箭头指示)。
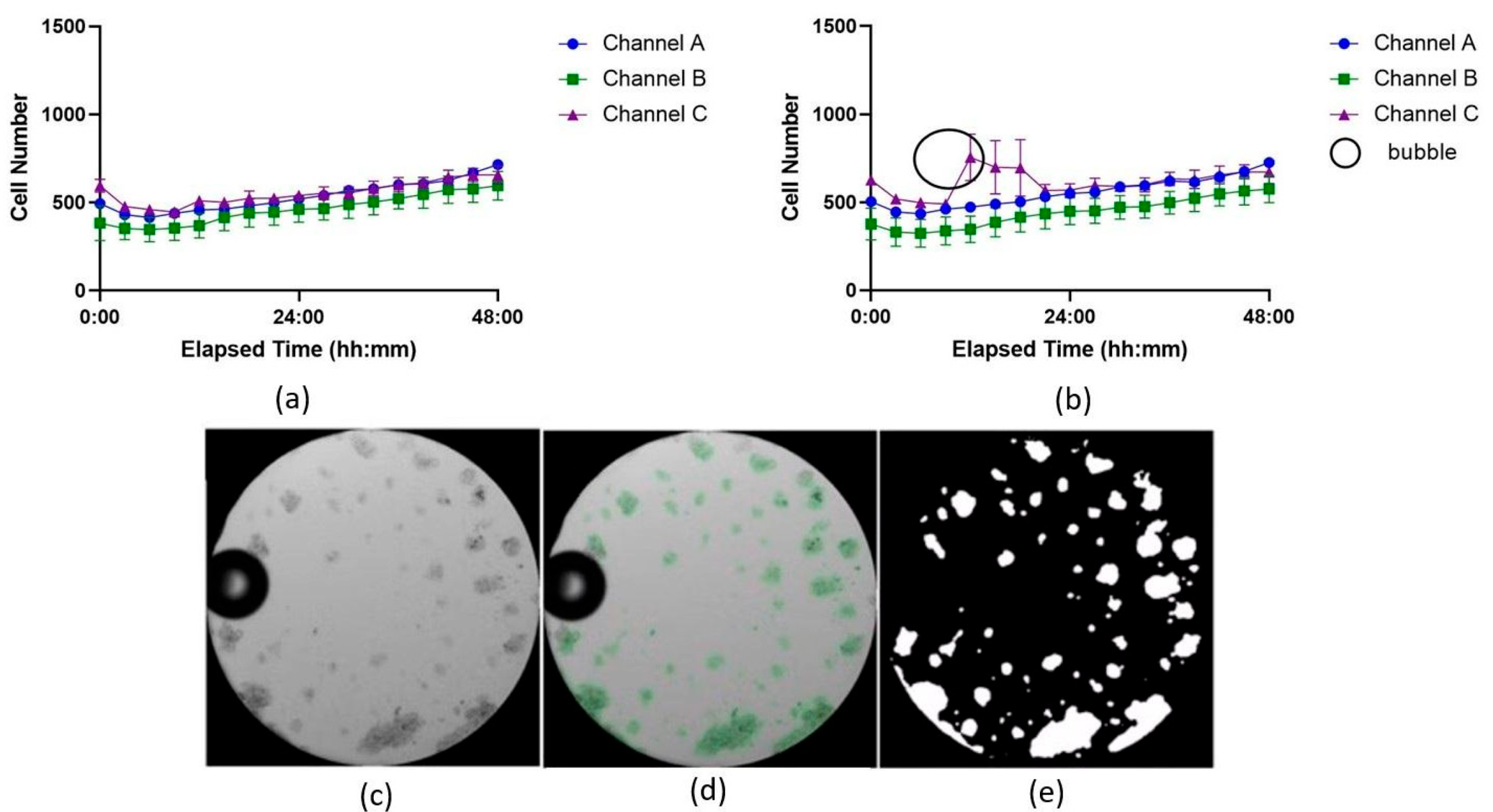
图 4. 用两种图像分析工具分析的细胞随时间增殖的生长曲线:(a)U-Net 模型和(b)Fiji 的可训练 WEKA 分割(TWS)插件。ibidi LOC 的三个独立通道作为技术重复,在相同条件下培养 Jurkat 细胞,并在此处分别标记为通道 A、B 和 C。每个时间点代表 7 个孔的平均值,其变化以平均值的标准误差(SEM)表示。在(b)中,大多数时间点的更高 SEM 变异表明其准确性低于(a)。黑色圆圈突出显示了被 TWS 错误识别为细胞区域的气泡阴影。(c)显微镜图像显示气泡。(d)U-Net 掩码突出显示细胞作为感兴趣区域。(e)U-Net 模型检测到的区域,不包括气泡作为细胞区域。

图 5. (a)定制的 PDMS 微流控芯片和(b)来自 ibidi® 的 μ-Slide 球体灌注芯片。
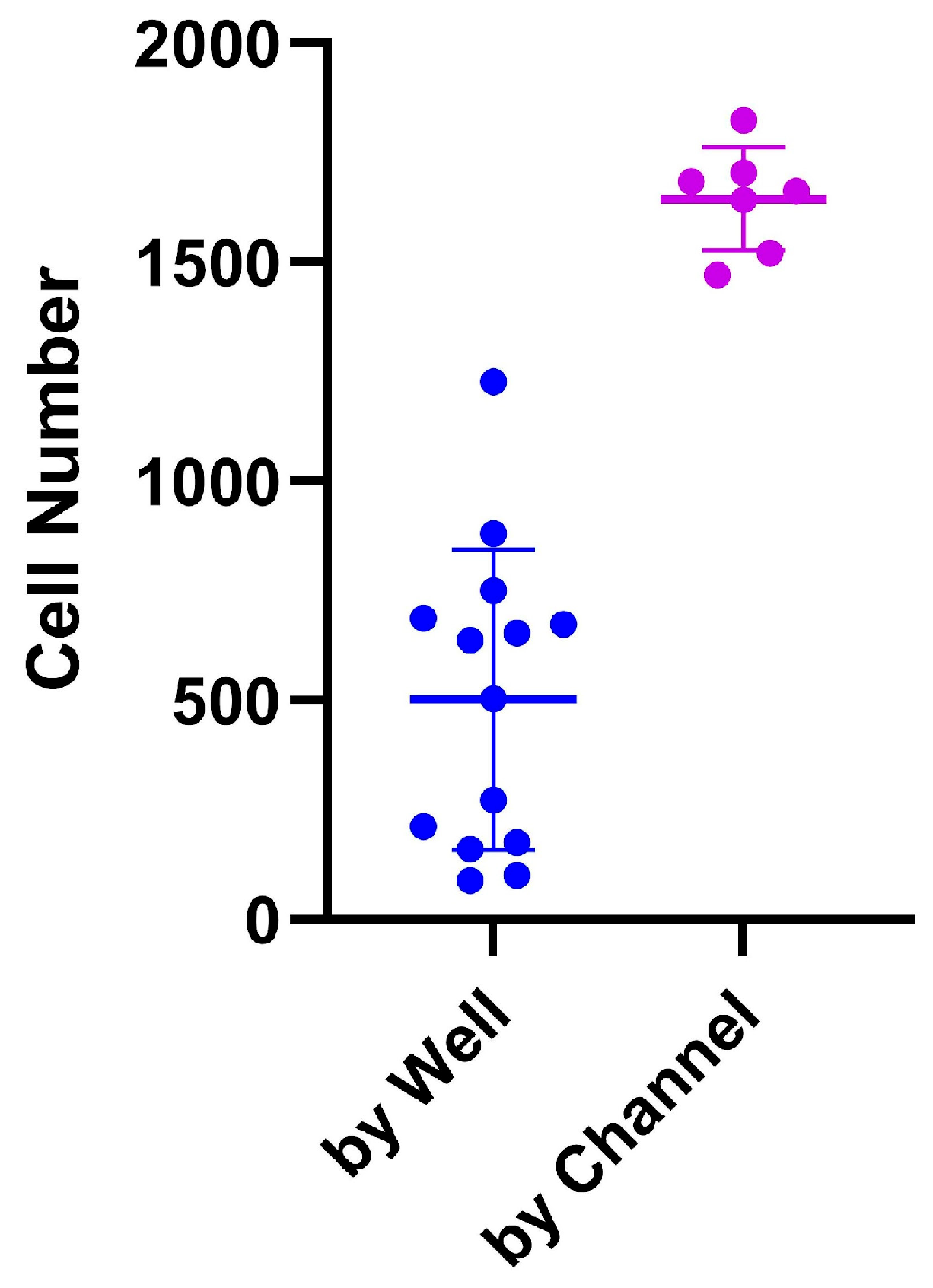
图 6. 在 ibidi LOC 中两种接种方案的比较:按孔接种和按通道接种。与按通道接种相比,按孔接种的细胞数量变化更大,而按通道接种的结果更一致。变化程度以标准差(SD)表示。
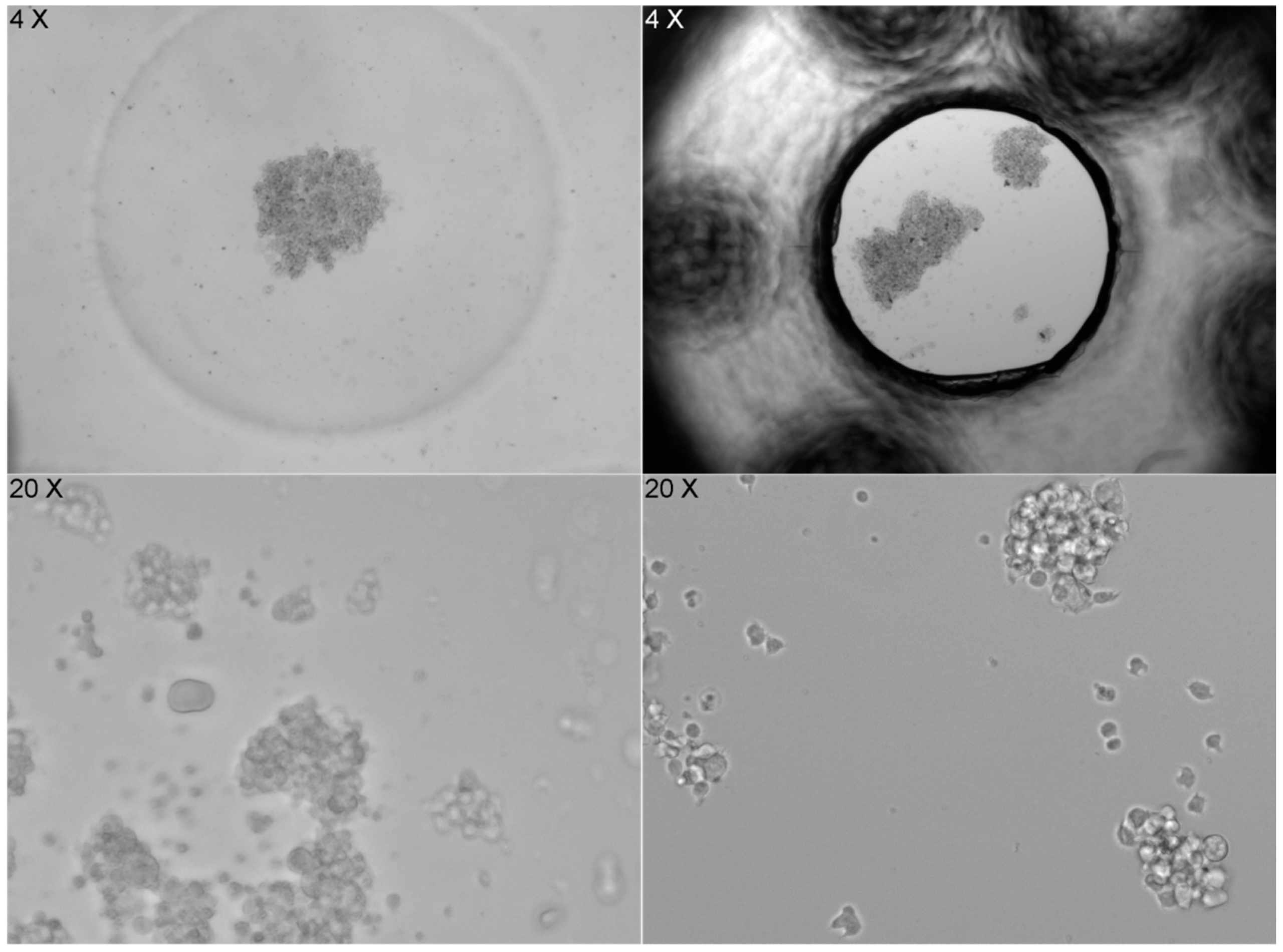
图 7. 比较两种不同 LOC 装置中细胞分布情况的图像序列。左侧为具有凹形(U 形)底部的 PDMS LOC 的图像,在 4 倍放大下,细胞在中心聚集,分布更均匀。然而,在 20 倍放大下,由于缺乏平坦表面,细胞无法清晰对焦。右侧为底部平坦的 ibidi LOC 的图像,在 4 倍放大下,细胞分布随机且不均匀,但在 20 倍放大下,图像清晰锐利,便于对焦。对比突出了底部表面形状对细胞分布和成像清晰度的影响。
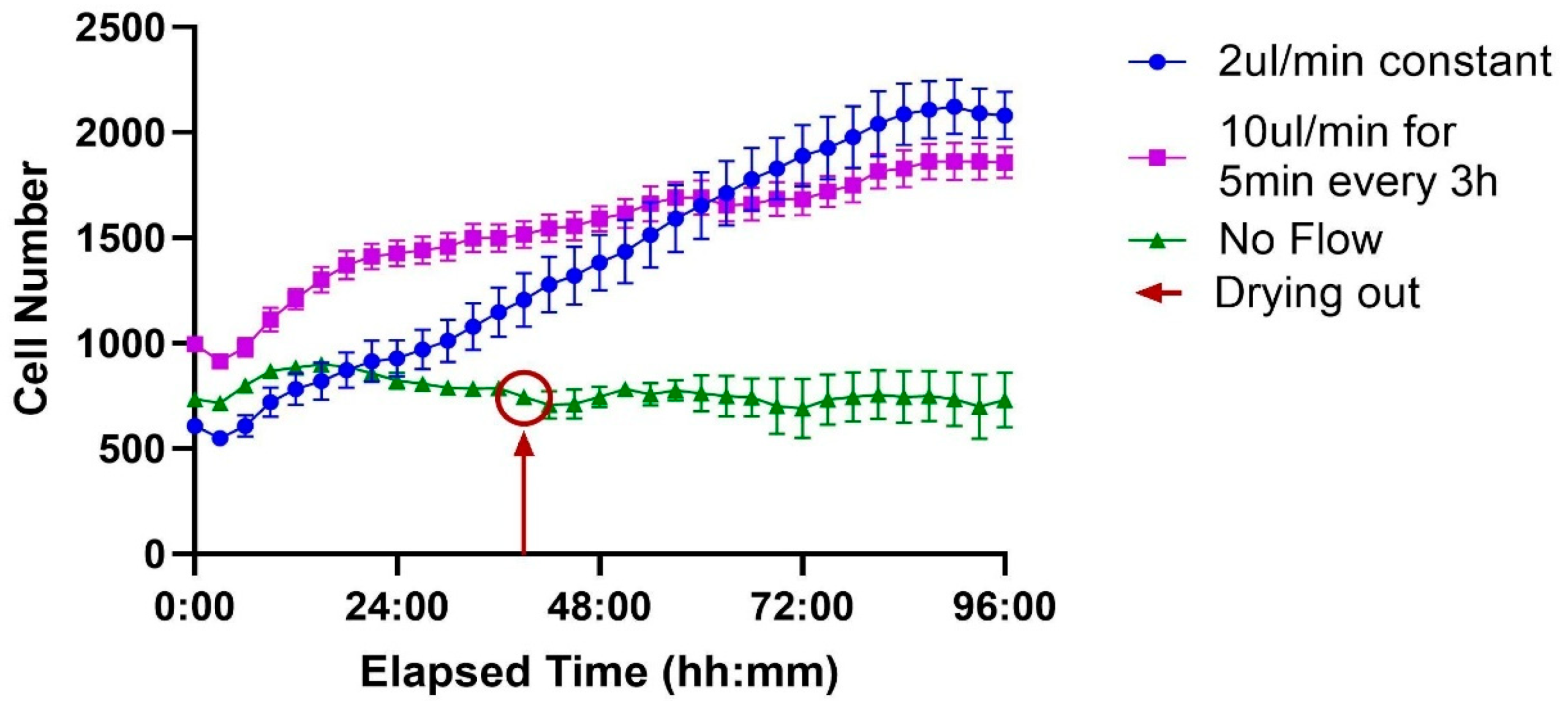
图 8. 流动条件对细胞增殖随时间变化的影响。比较了三种条件,分别在 ibidi LOC 的不同通道中进行:无流动、恒定流速为 2 μL/min以及每 3 小时间歇流动 10 μL/min 持续 5 min。无流动条件下细胞不增殖,红色圆圈表示通道开始干燥的时刻。相比之下,恒定流动和间歇流动条件均支持细胞的稳健生长,增殖率相似。每个时间点代表 7 个孔的平均值,标准误差(SEM)显示了其变化情况。
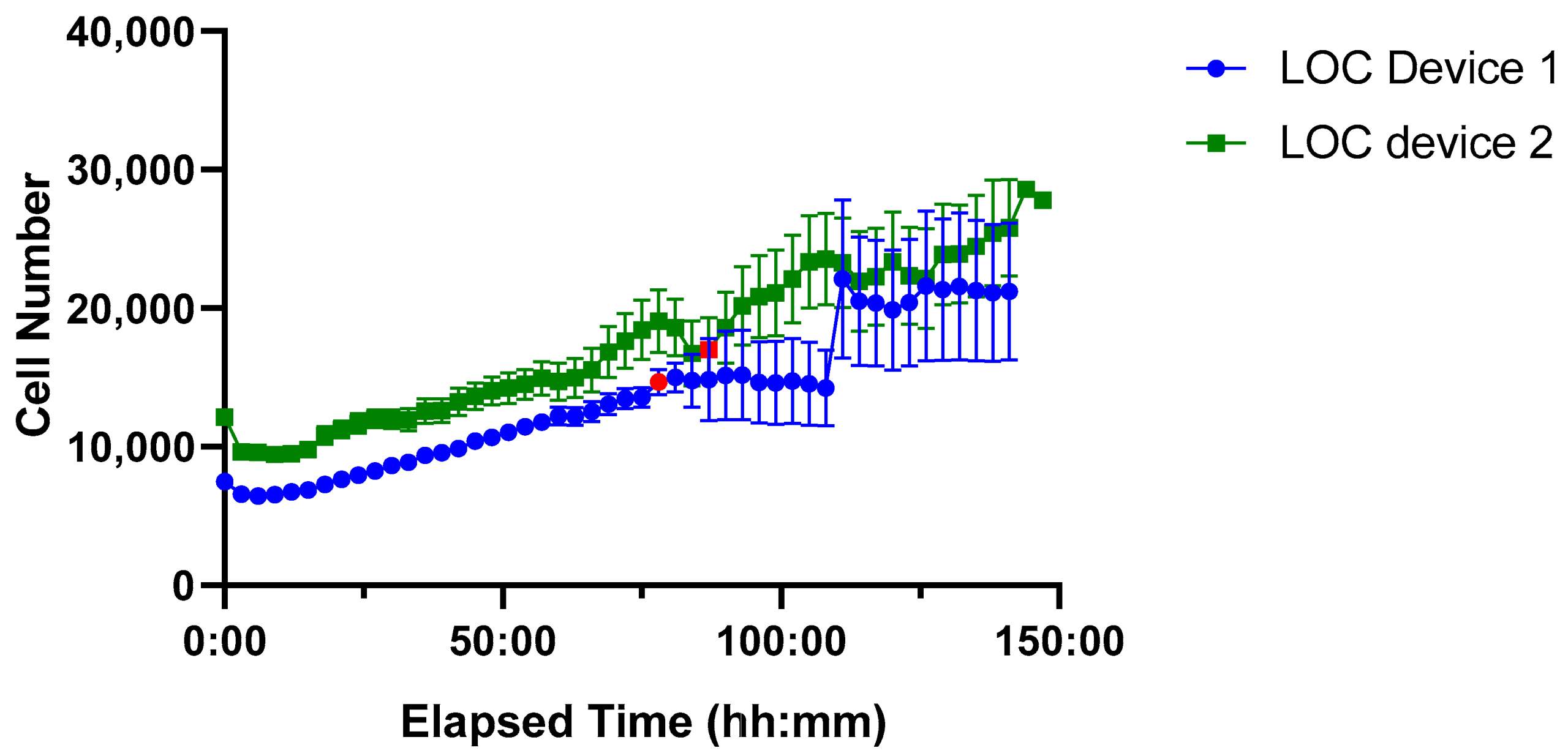
图 9. 两种聚二甲基硅氧烷(PDMS)微流控芯片中 Jurkat 细胞约 150 小时内的增殖时间进程。装置 1(蓝色线,圆形标记)和装置 2(绿色线,方形标记)均显示细胞持续生长且变异度低,直至出现干燥迹象(以红色标记表示)。每个数据点代表每个装置的平均细胞数,误差线表示平均值的标准误差(SEM)。
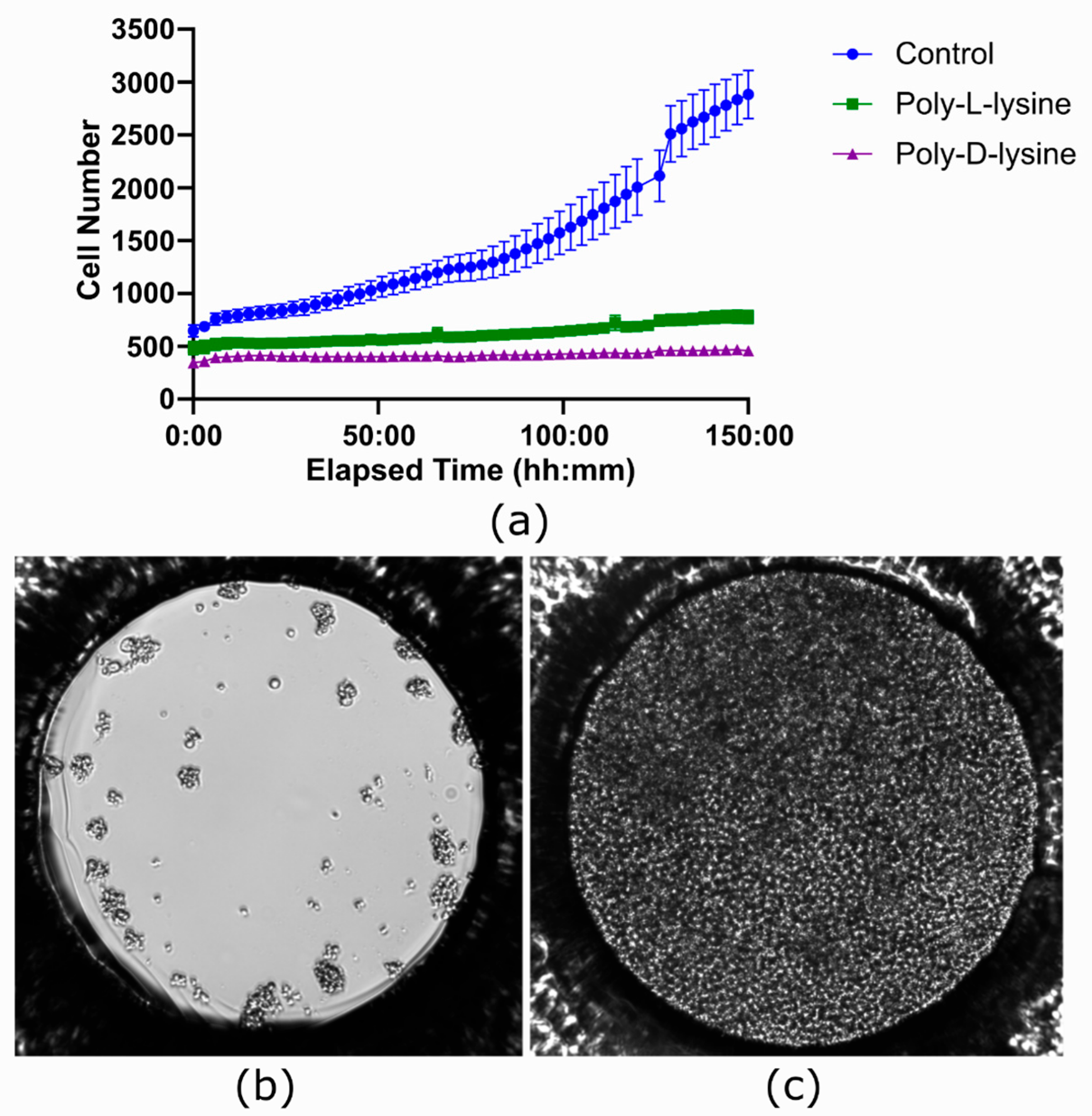
图 10. 聚赖氨酸在 ibidi LOC 中的包被效果。(a)比较三种条件下的生长曲线,每种条件分别在 ibidi LOC 的不同通道中进行:聚-L-赖氨酸包被、聚-D-赖氨酸包被以及未包被作为对照。在包被的通道中未观察到细胞增殖,而未包被的通道中 Jurkat 细胞有显著增殖。每个时间点代表 7 个孔的平均值,标准误差(SEM)显示了变化情况。(b)实验开始时拍摄的图像,显示细胞的初始状态。(c)实验结束时拍摄的图像,未包被孔的整个表面都被细胞覆盖。
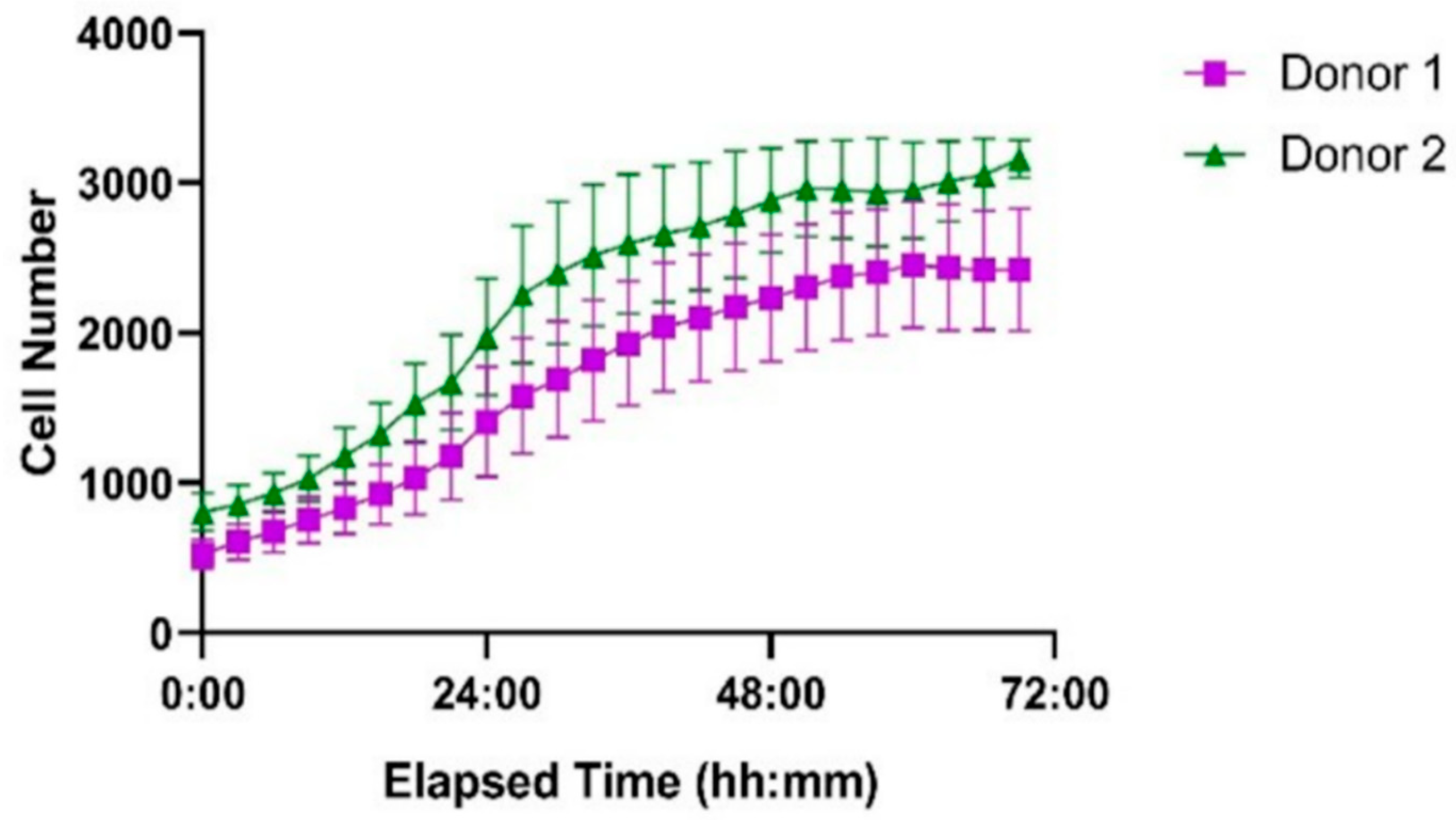
图 11. 两位健康供体的原代人 T 细胞在 ibidi LOC 中 72 小时内的增殖情况。细胞以相同的初始密度接种。供体 1(紫色方块)和供体 2(绿色三角形)均表现出成功的增殖,其中供体 2 的生长速率更高。每个点代表每个时间点的平均细胞数,误差线表示基于七个孔测量值的平均值的标准误差(SEM)。
与注射泵或蠕动泵等其他系统相比,这里介绍的微流控系统具有若干优势。尤其值得一提的是,它能够输送小体积的液体,最小流量为每分钟 2 μL,同时保持精确、无脉冲的流量控制以及高达 35 ms的响应时间。这种精度和一致性对于确保实验条件的准确性至关重要,特别是在生物检测中,流量扰动可能会影响细胞行为或破坏微环境的稳定性。无脉冲流动尤其有利,因为它可防止可能引入的剪切应力或营养物质及试剂分布不均的情况,从而提高实验结果的可靠性和可重复性。此外,在该装置中加入多路复用阀能够实现多种功能,包括试剂注入、程序灌注以及在微流控实验中的顺序输送。该系统能够在不到 156 ms的时间内,从多达 12 个独立的储液器中向单个微流控线路注入不同的液体样本,或者将一个液体样本输送至 12 个不同的微流控线路。
图像分析中的一个关键实际考量在于对计算资源的需求。虽然像 U-Net 这样的模型需要强大的 GPU,但我们的研究结果表明,现代的 YOLOv8 架构在效率更高的情况下实现了相当的性能。这使得无需专用硬件即可进行高级的本地图像分析成为可能。这一发现表明,基于深度学习的高质量分析正变得越来越容易获取。这与像 TWS 这样的工具的成功相类似,由于其在标准 CPU 上的可用性,TWS 得到了广泛的应用。然而,深度学习模型具有一个关键优势:性能更优。虽然 TWS 为机器学习提供了一个入门途径,但像 YOLOv8 这样的架构在准确性方面比这些传统方法有了显著的提升。因此,通过降低硬件要求,像 YOLOv8 这样高效的模型对于没有 IT 背景的研究人员来说也变得更加容易获取。
除了性能之外,深度学习模型在自动化和效率方面也具有明显的优势。一旦训练完成,深度学习模型就能完全自动地对新图像进行分割,从而省去了通常在每次实验中为优化 TWS 结果而进行的手动校正步骤。这种自动化不仅减少了分析时间,还通过消除用户依赖性变异性提高了可重复性。此外,诸如迭代自训练之类的高级深度学习策略,能够显著减少构建稳健模型所需的初始手动标注工作量。
在可用性方面,TWS 目前提供了更集成的训练流程。不过,随着新工具的出现,用于简化像 YOLO 这样的模型工作流程的差距正在缩小。例如,未来带有预训练 YOLO 模型的 Fiji 插件将进一步提高可访问性。本研究中模型的一个局限性在于其特定设备的训练;将其应用于不同的光学系统时,需要重新训练以确保最佳性能。
基于深度学习的分析可以扩展到包含更多的视觉指标,例如细胞的圆度和亮度,这些指标对于检测细胞形态的细微变化至关重要。这些指标在高倍放大实验中尤其有价值,因为它们能为细胞健康、激活和存活提供关键见解。
微流控芯片(LOC)器件在细胞培养方面具有显著优势,其利用微室使细胞能够沉降在孔底。这种设计确保了培养基可以更新而不会将细胞冲走或移位,这是传统悬浮培养方法中常见的难题。通过扩散为细胞提供营养和氧气,有效地维持了微流控芯片设备微环境中细胞的存活和增殖,这一点已得到先前研究的支持。
微流控芯片器件的另一个关键优势是其紧凑的尺寸,这与传统细胞培养方法相比,能减少试剂的消耗。例如,在标准的 96 孔板中,每个孔需要 200 μL培养基,因此每块板至少需要 19.2 mL培养基。相比之下,PDMS LOC 显著减少了这一用量,每个装置仅需 200 μL培养基,而 ibidi LOC 则进一步将每个通道的消耗量降至 45 μL,每个装置总共 135 μL。培养基用量的大幅减少不仅降低了实验成本,还提高了试剂的使用效率,这对于长期实验或涉及昂贵或稀缺材料的研究尤其有利。
流速是微流控系统中基于悬浮培养的 T 细胞等细胞培养的关键参数。我们实验中所用的 MFS 流量传感器的最低稳定且可精确测量的流速为 2 μL/min,因此选择此流速作为恒定流速。我们测试了这种连续灌注,以确定尽管其消耗更多培养基,但持续供应新鲜培养基是否能显著提高 T 细胞的增殖能力,与间歇供应相比。结果表明,尽管两种灌注策略都显著优于静态无流控制组,但恒定灌注和间歇灌注在最终细胞数量上没有统计学上的显著差异。这表明两种方法都能有效增强营养物质和废物的交换。恒定流速可能提供稳定的供应,而间歇脉冲可能通过定期冲洗系统来“重置”局部环境。关键的是,间歇灌注消耗的培养基不到恒定灌注的七分之一。鉴于这种相当的效力,间歇灌注成为更优且资源利用效率更高的策略,以实现稳健的 T 细胞扩增。
在我们的微流控系统中,用聚-D(L)-赖氨酸进行涂层提高了成像稳定性,但对细胞增殖产生了负面影响,这表明其弊端超过了预期的好处。聚赖氨酸是一种合成的带正电荷的聚合物,以其强大的细胞捕获特性而闻名,因此在悬浮细胞实验中常被用于促进细胞黏附。通过用这种聚合物涂覆表面,正电荷分子与带负电荷的细胞膜之间的相互作用得以促进,从而增强细胞附着。这在显微镜成像和长期研究中特别有益,因为它提高了细胞的可见度和稳定性。
然而,近期的研究表明,尽管聚赖氨酸被认为是一种惰性化合物,但它可能会无意中改变膜蛋白(如 T 细胞抗原受体(TCR))的活性,并妨碍正常的细胞过程。具体而言,其使细胞附着于培养通道底部的倾向可能会抑制玫瑰花结样结构的形成,从而损害细胞接收邻近细胞信号的能力,这可能导致细胞增殖减缓。关于细胞活力,研究表明聚-L-赖氨酸可诱导多种人类细胞类型发生明显的线粒体依赖性细胞凋亡。此外,这种聚合物的细胞毒性作用与处理时间和浓度相关,鉴于我们实验设置的长期性,这可能会对细胞产生显著影响。而且,由于 Jurkat 细胞处于悬浮状态,附着于表面可能会使细胞变形并改变其正常功能,从而可能导致细胞死亡。
这表明,尽管聚赖氨酸能够增强细胞黏附并防止在基于流动或灌注的实验中细胞被冲走,但在某些条件下它也可能阻碍细胞生长。在我们的系统中,图像稳定性并非限制因素,因为整个孔都能被捕捉到,而且由于 LOC 器件的设计,细胞冲走现象并未发生。鉴于细胞增殖受到抑制,因此弃用了聚赖氨酸。这突显了在实验设计中仔细考虑聚赖氨酸影响的必要性,尤其是在旨在促进细胞稳健生长和增殖的情况下。
本研究中展示的微流控系统通过成功支持两种细胞系和原代细胞,证明了其多功能性。这种能力在免疫治疗研究中尤其有利,因为使用原代细胞对于构建更准确的人类免疫反应模型至关重要。未来的研究将通过评估在这些设备中培养细胞后的细胞杀伤效率作为功能读出,来拓展所展示的 LOC 器件的潜在应用。这将为这些设备在需要细胞毒性检测的条件下(如药物筛选或免疫治疗研究)的表现提供宝贵的见解。此类功能评估对于确定这些设备在实际治疗应用中的转化相关性至关重要。
这项研究突显了采用压力驱动流控技术的自动化微流控系统所带来的显著进步,提高了生物检测的精度和一致性。压力控制器和流量传感器的集成,结合优化的控制参数,确保了稳定的流体条件,这对于维持细胞行为和微环境的稳定性至关重要。该系统能够以无脉冲流的方式输送小体积液体,从而减少剪切应力和营养物质分布的不均,进而提高实验结果的可靠性和可重复性。此外,基于深度学习的图像分析软件的使用,减少了结果的变异性,缩短了分析时间,并降低了假阳性的发生率。这些优势表明,在需要高精度和一致性细胞定量的实验中,深度学习工具可能会成为图像分析的首选。该系统的一个关键特性是使用了专门设计的 LOC 器件,使悬浮细胞能够在孔底沉淀。这种设计能够在不冲洗细胞的情况下实现培养基的更新,这对于悬浮细胞的长期实验来说特别有利。这些设备在细胞培养应用中具有独特的优势,能够确保长期稳定的条件并保持细胞活力。关于本研究中展示的 LOC 器件,PDMS LOC 便于多次重复实验,提高了可重复性。在优化条件下,其支持的细胞增殖程度也高于 ibidi LOC。另一方面,ibidi LOC 具有更大的灵活性,能够同时测试三种不同的条件,并允许细胞回收,这对于下游分析至关重要。总体而言,这些发现强调了选择合适的 LOC 设备以符合特定研究目标的重要性,为细胞生物学中的更有效实验设计铺平了道路。
参考文献:
Cadena Vizuete, M.F.; Condor, M.; Raith, D.; Sapre, A.; Follo, M.; Layedra, G.; Mertelsmann, R.; Perez, M.; Lerner, B. Biosensors 2025, 15, 693.
