��������ҩ���Ʊ�ϵͳ��mRNA-LNP������


������������ϳ�
����ͨ����ͨ����100 ��L/min��30 mL/min������������������֬������������PLGA���������ۺ����������ȡ�
�����õ�����ϵͳ
���伴��������ʵ��װ�ú�ʵ�������Ȼ��ʼʵ��
���߶ȿ��ظ����Զ�������������
���������ڵ��Զ���ʵ��������������25 nm��300 nm�ĸ߶ȵ���ɢ�������ӣ�PDI��0.20����
�����з��䷽������������ģ
ʹ����ͬ��������װ����������L���� L����������Һ��֬����������Һ��
����װ�Ķ���;��
ͨ��������ͬ��������оƬ��ʵ�ֲ�ͬ��ʵ����Ŀ�絥��Һ�κ�˫��Һ�β�������������ˮ�����顢�⽺�����;ۺ��������ϳɡ�����֬���塢PLGA��������20��1000��������PLGA��PVA��3Dϸ��������ϸ���������������������ݲ����ȡ�
�����������ϳ���װ�������ںϳɾ������õ���ɢ�ԣ���ͨ���Ϳ������Ե�������������������������߾���ѹ����������оƬ������װ�����ںϳɵ���ɢֱ��С��25 nm��֬������������ͨ��������ͬ��������оƬ��ͬʱ���������豸���䣬�������Ժϳɵ���ɢֱ����С��10 nm������������Ҫ�����Լ��䷽�Ż�����
���ڿ���ȷ��OB1��������������Һ������оƬ���봫ͳ��ʵ����ʵ����ȣ�����װ��������������������ĺϳ�ʱ��ͼ������Լ����ġ�
�����������Ӻϳ�
���������������ϳ���װ������ͨ��ѹ��������OB1 MK3+��ѹ��ͨ�������������嶯�����۽���ʵ���������ϳɹ�������������ֻ�ѧ��Һ���������������ϳ������ܿص����׳��������巴Ӧ���ȶ��ԺͶ���ѧֱ��ȡ��������ͨ���е�ÿ���������١�
ͨ�����������������MFS��BFS�����Բ����͵��ڹ�·�е�Һ��������
�������׳�����������ʵ�����õ�ͨ��������ɢ���Լ��ɵ�������������ͨ�����Ը��õؿ����������ĺϳɡ��йظ�����Ϣ�����Ķ����Ƕ��������������ϳɵ����ۣ�https://www.elveflow.com/microfluidic-reviews/general-microfluidics/microfluidic-nanoparticle-synthesis-short-review/������PLGA���׳��������ۣ�https://www.elveflow.com/microfluidic-reviews/general-microfluidics/microfluidics-for-plga-nanoparticle-synthesis-a-review/����
�����װ��ȷ����ͬ���֮��ľ������õļ����ԣ��������弴�õķ������ɵ������ƻ��������ƣ���������������ͬ��ʵ�顣�������������ϳ���װ���ʺϳ�ѧ�ߣ�Ҳ�ʺ�ר���û���
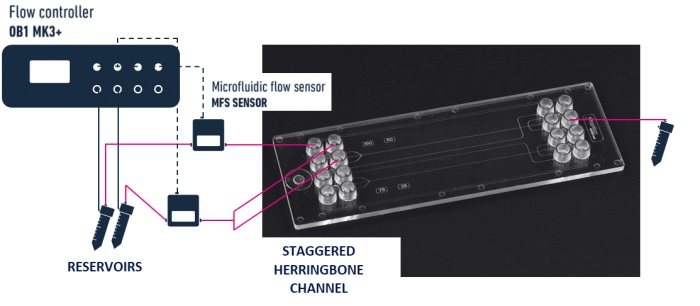
����������������֬����ϳ���װ������
1��2ͨ��OB1 MK3+����������
2��2��MFS��MFS4&MFS5��������������1��MFS5������������1����ʽBFS2������
3��2����Һ��
4��1�����������λ����оƬ
5�����������PTFE���ܡ�����������ͷ��������
6��ESI��������
Ϊʲôʹ�����������������
���ڿɾ�ϸ��������������ԣ�ʹ�����弼���ϳ��������ǽ���������ֱ����ɢ�Եĺ÷������dz���Ķ���ѧ��������ϳɾۺ����������Ľᾧ�ͳ�������Ҳ�Ƿdz���Ҫ�ġ�
���⣬���弼���Ǽ����������ϳ������DZ���м�ֵ��Ʒ��һ�ַ�����
�ܶ���֮����ʱ�䡢���ʺͷ�ɢ�Զ��ԣ�ʹ�����弼���ϳ��������Ⱥ�۵Ĵ�ͳʵ��ϳɸ�����Ч����������оƬ�Ѿ�С�ͻ�����ˣ������ڸ����ӵ�ʵ��ƽ̨��ʵʩ�������Ӻϳ���֣���ִ�и����Ҷ�ܵļ��ɹ��̡�
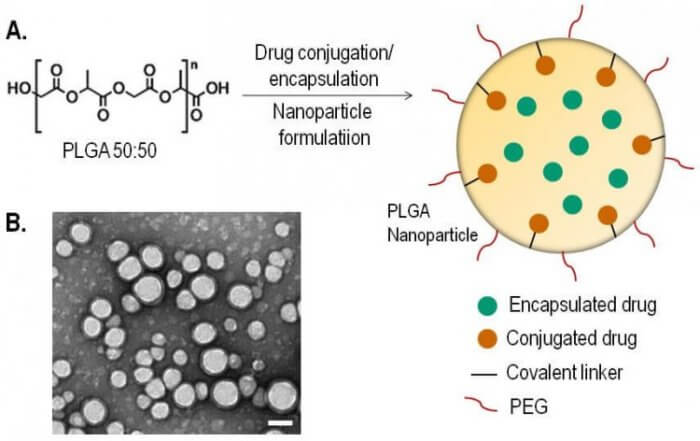
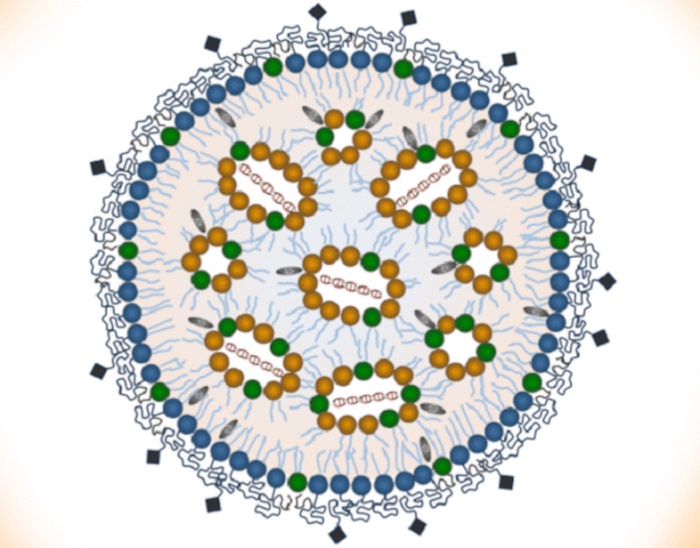
PLGA�������ӣ���A����PEG���ε�PLGA���������л�ѧż����ѧ���Ƽ��ļ�װ����B��PLGA�������ӵ�TEMͼ��Scale bar: 100 nm [1]
[1] Banerjee D, Harfouche R, Sengupta S. Nanotechnology-mediated targeting of tumor angiogenesis. Vasc Cell. 2011 Jan 31, 3(1), 3
�������������������֬����Ŀɵ��ڲ�����
1��������FRR�������������������仯��FRR=����������/����������
2��������TFR�仯��TFR=����������+����������
3��оƬ����--�������
4��֬�ʱ���--֬�����͡�֬��Ũ�ȡ�֬�ʱ��ʵ�
5��������Χ�ɵ����ɿ�
6��������--����ҩ����90%
7���з������������Ľ��һ���Ը�
Ӧ��
������Һ�����������׳���ԭ��
�Ѿ���ʾ�����弼�����ںϳɾ��пɵ���״�ͳߴ���л��������������ر�����[1]��������ʹ�������������ϳ���װʵ�֡����¶��ϡ����������ϳɷ������÷���ͨ�����������Σ��ɾۺϵ�����ɵ��������ɺˣ�ͨ�������ľۼ���ʹ���������ﵽƽ��[2-3]���봫ͳ�ĺ��ʵ��ϳ���ȣ�����ϳ����������и��õIJ��ʺ��õĿɵ�����[4]��
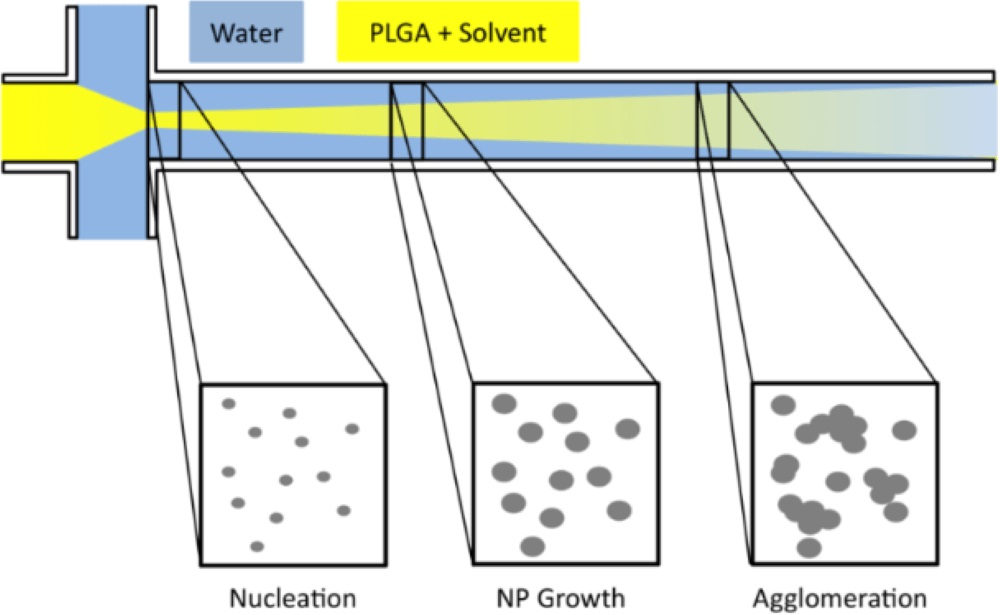
��PLGA���׳���Ϊ����PLGA�����ܽ����л��ܼ��У���оƬ���м�ͨ�����������Լ���ϵ�ˮ��Һע�뵽оƬ������ͨ���У��Ծ۽�PLGA��������ͨ����ɢ�γ�Ũ���ݶȺ�PLGA��������������ΪPLGA���Ӳ�����ˮ[5]��
���Ѿ�ʹ�����ؼ����ϳ����������������������ڱ�������ӹ���P4SPR���Ľ���������[6]�� �۶���Ȳ������[7]��
1. Ma, J., et al., Controllable synthesis of functional nanoparticles by microfluidic platforms for biomedical applications �C a review. Lab Chip, 2017. 17(2): p. 209-226.
2. Karnik, R., et al., Microfluidic platform for controlled synthesis of polymeric nanoparticles. Nano Lett, 2008. 8(9): p. 2906-12.
3. Lababidi, N., Sigal, V., Koenneke, A., Schwarzkopf, K., Manz, A., & Schneider, M. (2019). Microfluidics as tool to prepare size-tunable PLGA nanoparticles with high curcumin encapsulation for efficient mucus penetration. Beilstein Journal of Nanotechnology, 10, 2280�C2293.
4. Visaveliya, N. and J.M. Köhler, Single-step microfluidic synthesis of various nonspherical polymer nanoparticles via in situ assembling: dominating role of polyelectrolytes molecules. ACS Appl Mater Interfaces, 2014. 6(14): p. 11254-64.
5. Donno, R., Gennari, A., Lallana, E., De La Rosa, J. M. R., D��Arcy, R., Treacher, K., Hill, K., Ashford, M., & Tirelli, N. (2017). Nanomanufacturing through microfluidic- assisted nanoprecipitation: Advanced analytics and structure-activity relationships. International Journal of Pharmaceutics, 534(1�C2), 97�C107.
6. Boken, J., D. Kumar, and S. Dalela, Synthesis of Nanoparticles for Plasmonics Applications: A Microfluidic Approach. Synthesis and Reactivity in Inorganic, Metal- Organic, and Nano-Metal Chemistry, 2015. 45(8): p. 1211-1223.
7. Baek, S., et al., Nanoscale diameter control of sensory polydiacetylene nanoparticles on microfluidic chip for enhanced fluorescence signal. Sensors and Actuators B: Chemical, 2016. 230: p. 623-629.
������������������������֬���������װ
����������/����֬����ϳ���װ�Ǹ߶ȿɶ��Ƶģ����Բ��ò�ͬ������оƬ�ϳɲ�ͬ����������������֬���塣���磬����оƬ�ϳɺ������ͨ���������и���ķ�Ӧ�ռ䡣
��Һ��оƬ�IJ�����PMMA��COP���ֲ��ϣ������ֲ��϶��ǹ�ѧ���ģ��������������������ϳ�Э������ݡ�
���⣬�����Ҫ�õ���ѹ��������ƣ������������е���װ�豸����������������������OB1������������OB1 DUAL��ѹ��ѹ���ܣ�ͬʱ��������ѡ��ͬ���Ĵ�Һ�����1.5 mL Eppendorf�ܵ�100 mL����ƿ����Ȼ����������ѡ���ʽ����������BFS������MFS���Խ�һ�������������ơ�
����������/����λ��оƬ����оƬ��Staggered Herringbone Micromixer glass chip -- SHM glass chip��

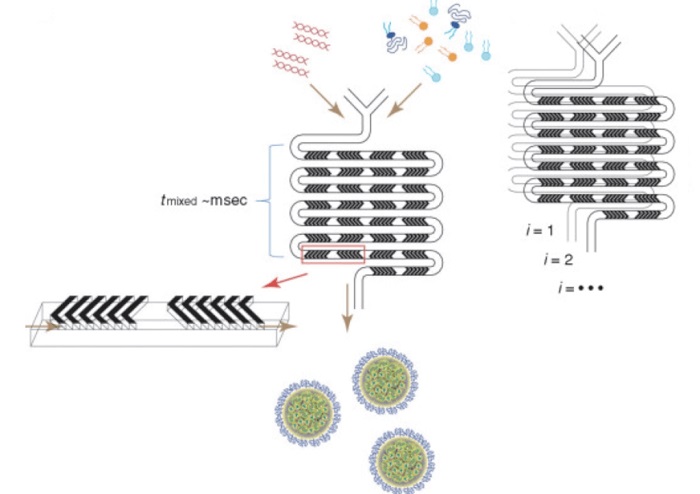
����λ��������оƬ��staggered herringbone micromixer glass chip -- SHM glass chip����һ�ֿ�����ͨ�������ͨ�����л��Һ���һ�����ù��ߡ�
��ͨ���Ͳ���оƬͨ��������ɢ����ij��Ȳ���������������֮�䴫��Ŀ����ԣ��Ӷ��ṩ��һ�ֿ��ٻ����������ķ�����
����������оƬʹ�÷��㡢���ÿɿ�����Ӧ������������ʵ�飺
�� ��ǿ�ȹ�ѧ������
�� �������ز�Ƭ�ߴ磨25��75 mm��
�� ��1/4-28UNF���ƶ˿�
�� ���ڴ���
�� ֻ��ʹ��1/4-28UNF��ͷ������������⾶1/16Ӣ��ĵ��ܣ���оƬ���ӵ�����װ�ü��ɡ�
����ԭ����Ӧ��
�����λ����ͨ���յ����������γɣ��ڵ���ŵ����������ʾ���ٻ�ϡ�
�����λ����оƬͨ���ײ����в��ԳƵ������ΰ��۵��ض�ͼ�����ð����ܹ����������������ڻ������Һ��Ļ��ҽ��衣
����ͨ��������Ļ�Ͼ��кܶ��Ӧ�ã����绯ѧ��Ӧ�������Լ���Һ�ľ��ʻ���
���������λ����оƬ�Ѿ���֬���壨��յ���֬���ݣ��IJ�����ȡ������Ҫ�Ľ�����Cheung���ˣ�Int J Pharma 2019��ȷʵ�״α�����ʹ�������λ����оƬ�����ȶ��Ҿ��ȵģ�100 nm�����Ҷ�����֬���塣�����о��˲�ͬ�䷽��ˮ��Һ����ʼ֬��Ũ�ȡ�֬�ʳɷֺ���֣����ղ�����Ӱ�졣
�����������豸��ȣ��û����оƬ��ʾ�����ߵ�ͨ��������Ļ�Ϻ�С��ϴ�ѡ�
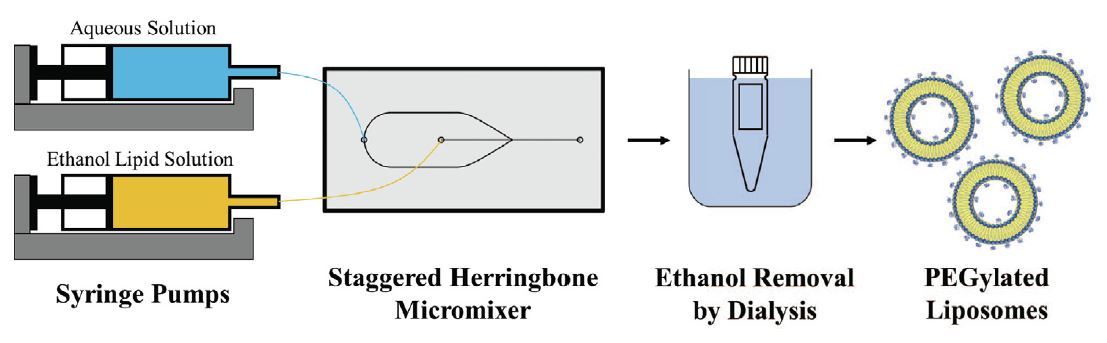
�����β������оƬ�Ĺ�����
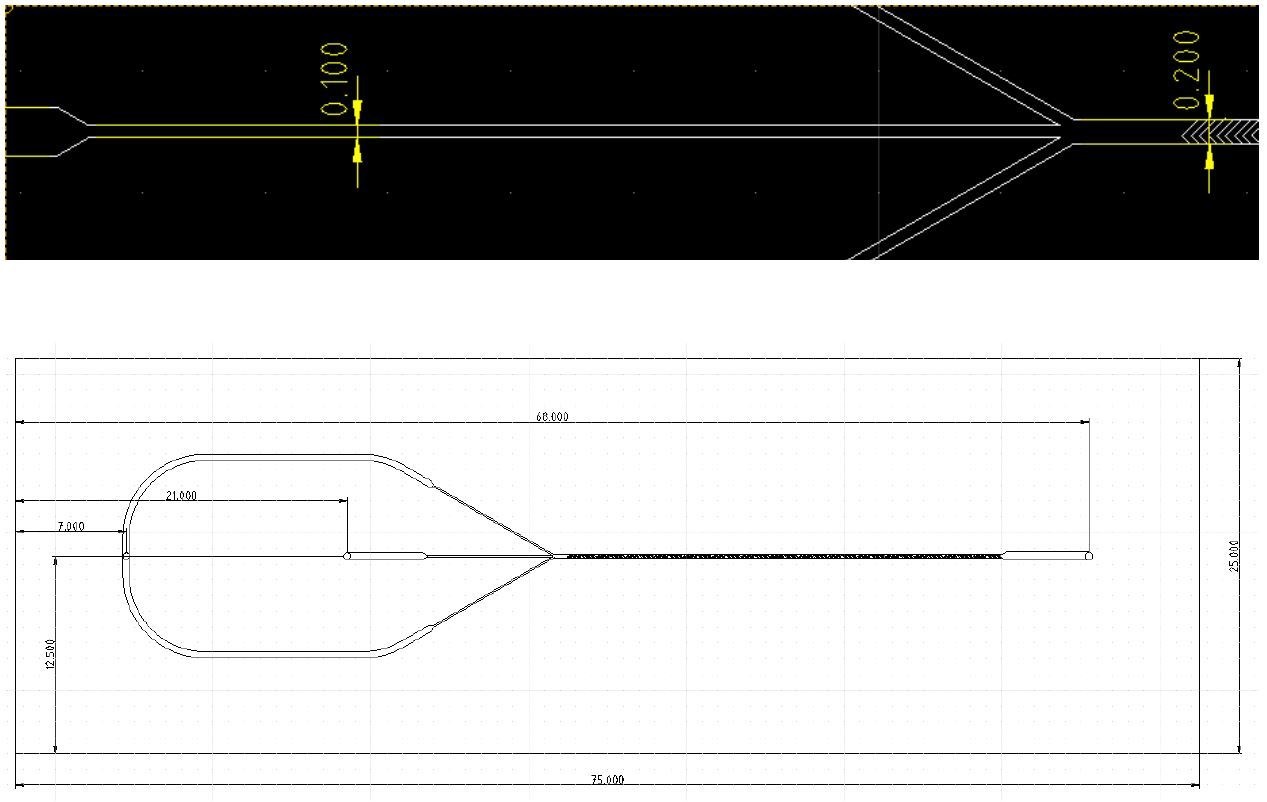
���Ⱥͳ��ȣ�25 ��75 mm
ͨ����ȣ�0.08 mm
ͨ�����ȣ�0.1��0.5 mm
�����3.3 ��L
��������0.47 ��L
��ϳ��ȣ�28.7 mm
���ʣ�����
��������1/4-28��ͷ
�ڻ�ϲ��֣���6�����Ԫ���������Σ��γ�һ���飨���ѭ������30���飬��ˣ��ܹ���15������ѭ�����û��оƬ��1��3bar��ѹ�������˲��ԣ���Ҳ������������10barѹ�����ԡ�
�� �����ε���������ͨ���ߴ磨200 ��m����1/3��2/3
�� ������֮��ľ�����50 ��m
�� ÿ�����Ԫ���Ŀ�����50 ��m���߶���30 ��m
�����
Calvin C.L.Cheung, Wafa T.Al-Jamal. Sterically stabilized liposomes production using staggered herringbone micromixer: Effect of lipid composition and PEG-lipid content. International Journal of Pharmaceutics, Volume 566, 20 July 2019, Pages 687-696. PDF������ here
�����Ը��ݾ����ʵ����Ŀ��������������������֬����ϳ�оƬ�������豸����䶯���ɳ���ʹ�á�
���ػ����оƬ���ܣ���� here
��Ʒ�������ӣ�
OB1 MK3+ -��ͨ������ѹ��&��տ���������ϸ���ܣ����� ����
ESI-��������ר�õ�����ͼ�λ����������������ϸ���ܣ����� ����
BFS-��������������������������У��ֱ�Ӳ���������ϸ���ܣ����� ����
MFS-������ʽ��������������ϸ���ܣ����� ����










